ਹਾਲ ਹੀ ਵਿੱਚ, ਤਿੰਨ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਨੂੰ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ ਹੈ, ਅਰਥਾਤ: (1) 21 ਜੁਲਾਈ, 2022 ਨੂੰ, ਪੀਟੀਸੀ ਥੈਰੇਪਿਊਟਿਕਸ, ਇੰਕ. (NASDAQ: PTCT) ਨੇ ਘੋਸ਼ਣਾ ਕੀਤੀ ਕਿ ਇਸਦੀ AAV ਜੀਨ ਥੈਰੇਪੀ Upstaza™ ਨੂੰ ਯੂਰਪੀਅਨ ਕਮਿਸ਼ਨ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ ਸੀ, ਇਹ ਪਹਿਲੀ ਮਾਰਕੀਟ ਕੀਤੀ ਗਈ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜੋ ਬ੍ਰੇਨ ਵਿੱਚ ਸਿੱਧਾ ਟੀਕਾ ਲਗਾਇਆ ਗਿਆ ਇੱਕ ਹੋਰ ਲੇਖ ਹੈ | ਦਿਮਾਗ ਵਿੱਚ ਸਿੱਧਾ ਟੀਕਾ ਲਗਾਉਣ ਵਾਲੀ ਥੈਰੇਪੀ ਨੂੰ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਜਾਂਦੀ ਹੈ)।(2) 17 ਅਗਸਤ, 2022 ਨੂੰ, ਯੂਐਸ ਫੂਡ ਐਂਡ ਡਰੱਗ ਐਡਮਨਿਸਟ੍ਰੇਸ਼ਨ (FDA) ਨੇ ਬੀਟਾ ਥੈਲੇਸੀਮੀਆ ਦੇ ਇਲਾਜ ਲਈ ਬਲੂਬਰਡ ਬਾਇਓ ਦੀ ਜੀਨ ਥੈਰੇਪੀ ਜ਼ਿੰਟੇਗਲੋ (ਬੇਟੀਬੇਗਲੋਜੀਨ ਆਟੋਟੇਮਸੇਲ, ਬੇਟੀ-ਸੇਲ) ਨੂੰ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ।ਸੰਯੁਕਤ ਰਾਜ ਵਿੱਚ ਥੈਰੇਪੀ ਦੀ ਮਨਜ਼ੂਰੀ ਨਿਰਸੰਦੇਹ ਬਲੂਬਰਡ ਬਾਇਓ ਲਈ "ਬਰਫ਼ ਵਿੱਚ ਮਦਦ" ਹੈ, ਜੋ ਵਿੱਤੀ ਸੰਕਟ ਵਿੱਚ ਹੈ।(3) 24 ਅਗਸਤ, 2022 ਨੂੰ, ਬਾਇਓਮੈਰਿਨ ਫਾਰਮਾਸਿਊਟੀਕਲ (ਬਾਇਓਮੈਰਿਨ) ਨੇ ਘੋਸ਼ਣਾ ਕੀਤੀ ਕਿ ਯੂਰਪੀਅਨ ਕਮਿਸ਼ਨ ਨੇ ROCTAVIAN™ (ਵੈਲੋਟੋਕੋਜੀਨ ਰੋਕਸਾਪਰਵੋਵੇਕ), ਹੀਮੋਫਿਲੀਆ ਏ ਲਈ ਇੱਕ ਜੀਨ ਥੈਰੇਪੀ ਦੀ ਸ਼ਰਤੀਆ ਮਾਰਕੀਟਿੰਗ ਨੂੰ ਮਨਜ਼ੂਰੀ ਦੇ ਦਿੱਤੀ ਹੈ, ਜੋ ਕਿ FVIII ਫੈਕਟਰ ਇਨਿਹਿਬਟਰਜ਼ ਦਾ ਕੋਈ ਇਤਿਹਾਸ ਨਹੀਂ ਵਾਲੇ ਮਰੀਜ਼ਾਂ ਦੇ ਇਲਾਜ ਲਈ ਹੈ: ਏ. ਬਾਇਓਮੈਰਿਨ ਦੀ ਹੀਮੋਫਿਲਿਆ ਏ ਜੀਨ ਥੈਰੇਪੀ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰ)।ਹੁਣ ਤੱਕ, 41 ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਨੂੰ ਦੁਨੀਆ ਭਰ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ ਹੈ।
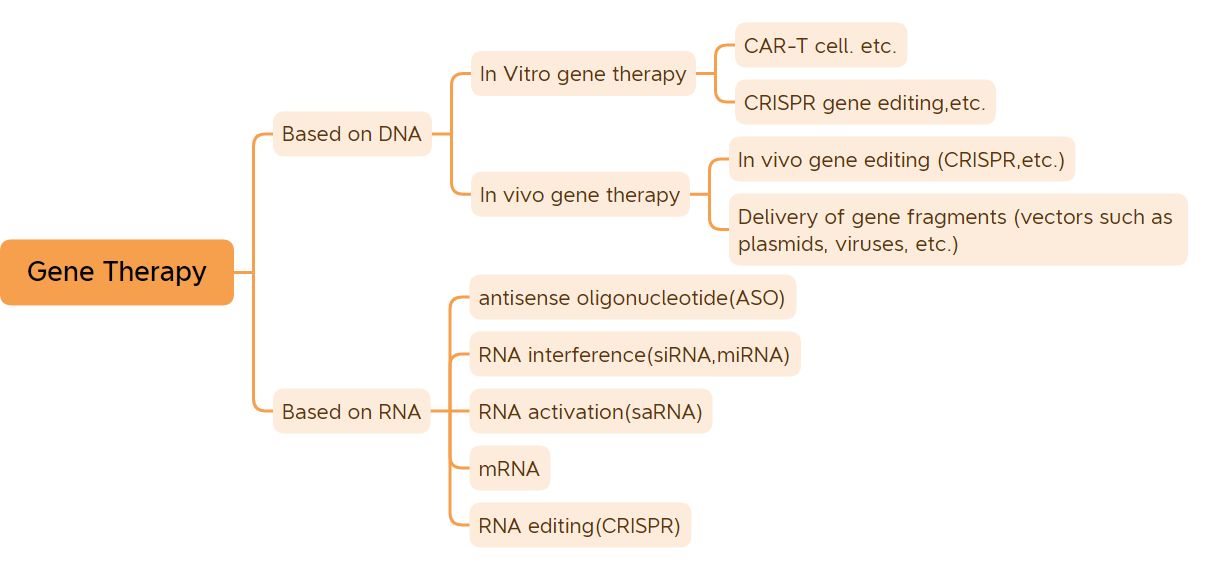
ਜੀਨ ਮੂਲ ਜੈਨੇਟਿਕ ਇਕਾਈ ਹੈ ਜੋ ਗੁਣਾਂ ਨੂੰ ਨਿਯੰਤਰਿਤ ਕਰਦੀ ਹੈ।ਕੁਝ ਵਾਇਰਸਾਂ ਦੇ ਜੀਨਾਂ ਨੂੰ ਛੱਡ ਕੇ, ਜੋ ਕਿ ਆਰਐਨਏ ਨਾਲ ਬਣੇ ਹੁੰਦੇ ਹਨ, ਜ਼ਿਆਦਾਤਰ ਜੀਵਾਂ ਦੇ ਜੀਨ ਡੀਐਨਏ ਨਾਲ ਬਣੇ ਹੁੰਦੇ ਹਨ।ਜੀਵ ਦੀਆਂ ਜ਼ਿਆਦਾਤਰ ਬਿਮਾਰੀਆਂ ਜੀਨਾਂ ਅਤੇ ਵਾਤਾਵਰਣ ਦੇ ਆਪਸੀ ਤਾਲਮੇਲ ਕਾਰਨ ਹੁੰਦੀਆਂ ਹਨ, ਅਤੇ ਬਹੁਤ ਸਾਰੀਆਂ ਬਿਮਾਰੀਆਂ ਨੂੰ ਜੀਨ ਥੈਰੇਪੀ ਦੁਆਰਾ ਸੰਖੇਪ ਵਿੱਚ ਠੀਕ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ ਜਾਂ ਦੂਰ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ।ਜੀਨ ਥੈਰੇਪੀ ਨੂੰ ਦਵਾਈ ਅਤੇ ਫਾਰਮੇਸੀ ਦੇ ਖੇਤਰ ਵਿੱਚ ਇੱਕ ਕ੍ਰਾਂਤੀ ਮੰਨਿਆ ਜਾਂਦਾ ਹੈ।ਵਿਆਪਕ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਵਿੱਚ ਡੀਐਨਏ-ਸੰਸ਼ੋਧਿਤ ਡੀਐਨਏ ਦਵਾਈਆਂ (ਜਿਵੇਂ ਕਿ ਵੀਵੋ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਵਿੱਚ ਵਾਇਰਲ ਵੈਕਟਰ-ਅਧਾਰਿਤ, ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ, ਨੰਗੀਆਂ ਪਲਾਜ਼ਮੀਡ ਦਵਾਈਆਂ, ਆਦਿ) ਅਤੇ ਆਰਐਨਏ ਦਵਾਈਆਂ (ਜਿਵੇਂ ਕਿ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਦਵਾਈਆਂ, ਅਤੇ ਐਮਆਰਐਨਏ, ਡਰੱਗਜ਼, ਐਮਆਰਐਨਏ, ਡਰੱਗਜ਼ ਆਦਿ) 'ਤੇ ਆਧਾਰਿਤ ਦਵਾਈਆਂ ਸ਼ਾਮਲ ਹਨ।ਸੰਖੇਪ ਰੂਪ ਵਿੱਚ ਪਰਿਭਾਸ਼ਿਤ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਵਿੱਚ ਮੁੱਖ ਤੌਰ 'ਤੇ ਪਲਾਜ਼ਮੀਡ ਡੀਐਨਏ ਦਵਾਈਆਂ, ਵਾਇਰਲ ਵੈਕਟਰਾਂ 'ਤੇ ਅਧਾਰਤ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ, ਬੈਕਟੀਰੀਅਲ ਵੈਕਟਰਾਂ 'ਤੇ ਅਧਾਰਤ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ, ਜੀਨ ਸੰਪਾਦਨ ਪ੍ਰਣਾਲੀਆਂ ਅਤੇ ਸੈੱਲ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਸ਼ਾਮਲ ਹੁੰਦੀਆਂ ਹਨ ਜੋ ਵਿਟਰੋ ਵਿੱਚ ਜੈਨੇਟਿਕ ਤੌਰ 'ਤੇ ਸੋਧੀਆਂ ਜਾਂਦੀਆਂ ਹਨ।ਸਾਲਾਂ ਦੇ ਕਠੋਰ ਵਿਕਾਸ ਦੇ ਬਾਅਦ, ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਨੇ ਪ੍ਰੇਰਣਾਦਾਇਕ ਕਲੀਨਿਕਲ ਨਤੀਜੇ ਪ੍ਰਾਪਤ ਕੀਤੇ ਹਨ।(DNA ਵੈਕਸੀਨ ਅਤੇ mRNA ਵੈਕਸੀਨਾਂ ਨੂੰ ਛੱਡ ਕੇ), 41 ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ ਨੂੰ ਵਿਸ਼ਵ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ ਹੈ।ਉਤਪਾਦਾਂ ਦੀ ਸ਼ੁਰੂਆਤ ਅਤੇ ਜੀਨ ਥੈਰੇਪੀ ਤਕਨਾਲੋਜੀ ਦੇ ਤੇਜ਼ੀ ਨਾਲ ਵਿਕਾਸ ਦੇ ਨਾਲ, ਜੀਨ ਥੈਰੇਪੀ ਤੇਜ਼ੀ ਨਾਲ ਵਿਕਾਸ ਦੇ ਦੌਰ ਦੀ ਸ਼ੁਰੂਆਤ ਕਰਨ ਵਾਲੀ ਹੈ।
ਜੀਨ ਥੈਰੇਪੀ ਦਾ ਵਰਗੀਕਰਨ (ਚਿੱਤਰ ਸਰੋਤ: ਜੀਵ ਜਿੰਗਵੇਈ)
ਇਹ ਲੇਖ 41 ਜੀਨ ਥੈਰੇਪੀਆਂ ਦੀ ਸੂਚੀ ਦਿੰਦਾ ਹੈ ਜਿਨ੍ਹਾਂ ਨੂੰ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ ਹੈ (DNA ਵੈਕਸੀਨਾਂ ਅਤੇ mRNA ਵੈਕਸੀਨਾਂ ਨੂੰ ਛੱਡ ਕੇ)।
1. ਇਨ ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ
(1) ਸਟ੍ਰੀਮਵੇਲਿਸ
ਕੰਪਨੀ: GlaxoSmithKline (GSK) ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਮਈ 2016 ਵਿੱਚ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਗੰਭੀਰ ਸੰਯੁਕਤ ਇਮਯੂਨੋਡਫੀਸ਼ੈਂਸੀ (SCID) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਇਸ ਥੈਰੇਪੀ ਦੀ ਆਮ ਪ੍ਰਕਿਰਿਆ ਪਹਿਲਾਂ ਮਰੀਜ਼ ਦੇ ਆਪਣੇ ਹੀਮੈਟੋਪੀਓਏਟਿਕ ਸਟੈਮ ਸੈੱਲਾਂ ਨੂੰ ਪ੍ਰਾਪਤ ਕਰਨਾ, ਵਿਟਰੋ ਵਿੱਚ ਉਹਨਾਂ ਦਾ ਵਿਸਤਾਰ ਅਤੇ ਸੰਸਕ੍ਰਿਤ ਕਰਨਾ ਹੈ, ਅਤੇ ਫਿਰ ਉਹਨਾਂ ਦੇ ਹੇਮੇਟੋਪੋਏਟਿਕ ਸਟੈਮ ਸੈੱਲਾਂ ਵਿੱਚ ਕਾਰਜਸ਼ੀਲ ADA (ਐਡੀਨੋਸਾਈਨ ਡੀਮਿਨੇਜ਼) ਜੀਨ ਦੀ ਇੱਕ ਕਾਪੀ ਪੇਸ਼ ਕਰਨ ਲਈ ਰੈਟਰੋਵਾਇਰਸ ਦੀ ਵਰਤੋਂ ਕਰਨਾ ਹੈ, ਅਤੇ ਅੰਤ ਵਿੱਚ ਸੰਸ਼ੋਧਿਤ ਹੇਮਾਟੋਪੀਓਏਟਿਕ ਸਟੈਮ ਸੈੱਲਾਂ ਨੂੰ ਤਬਦੀਲ ਕਰਨਾ ਹੈ।ਹੈਮੇਟੋਪੋਇਟਿਕ ਸਟੈਮ ਸੈੱਲਾਂ ਨੂੰ ਸਰੀਰ ਵਿੱਚ ਵਾਪਸ ਦਾਖਲ ਕੀਤਾ ਜਾਂਦਾ ਹੈ।ਕਲੀਨਿਕਲ ਨਤੀਜਿਆਂ ਨੇ ਦਿਖਾਇਆ ਕਿ ਸਟ੍ਰੀਮਵੇਲਿਸ ਨਾਲ ਇਲਾਜ ਕੀਤੇ ਗਏ ADA-SCID ਮਰੀਜ਼ਾਂ ਦੀ 3-ਸਾਲ ਦੀ ਬਚਣ ਦੀ ਦਰ 100% ਸੀ।
(2) ਜ਼ਲਮੋਕਸਿਸ
ਕੰਪਨੀ: ਮੋਲਮੇਡ, ਇਟਲੀ ਦੁਆਰਾ ਨਿਰਮਿਤ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2016 ਵਿੱਚ EU ਸ਼ਰਤੀਆ ਮਾਰਕੀਟਿੰਗ ਅਧਿਕਾਰ ਪ੍ਰਾਪਤ ਕੀਤਾ।
ਸੰਕੇਤ: ਇਹ ਹੈਮੇਟੋਪੋਏਟਿਕ ਸਟੈਮ ਸੈੱਲ ਟ੍ਰਾਂਸਪਲਾਂਟੇਸ਼ਨ ਤੋਂ ਬਾਅਦ ਮਰੀਜ਼ਾਂ ਦੀ ਇਮਿਊਨ ਸਿਸਟਮ ਦੀ ਸਹਾਇਕ ਥੈਰੇਪੀ ਲਈ ਵਰਤਿਆ ਜਾਂਦਾ ਹੈ।
ਟਿੱਪਣੀਆਂ: ਜ਼ੈਲਮੋਕਸਿਸ ਇੱਕ ਐਲੋਜੈਨਿਕ ਟੀ ਸੈੱਲ ਆਤਮਘਾਤੀ ਜੀਨ ਇਮਯੂਨੋਥੈਰੇਪੀ ਹੈ ਜੋ ਰੈਟਰੋਵਾਇਰਲ ਵੈਕਟਰ ਦੁਆਰਾ ਸੋਧਿਆ ਗਿਆ ਹੈ।1NGFR ਅਤੇ HSV-TK Mut2 ਆਤਮਘਾਤੀ ਜੀਨ ਲੋਕਾਂ ਨੂੰ ਕਿਸੇ ਵੀ ਸਮੇਂ ਟੀ ਸੈੱਲਾਂ ਨੂੰ ਮਾਰਨ ਲਈ ਗੈਨਸੀਕਲੋਵਿਰ ਦੀ ਵਰਤੋਂ ਕਰਨ ਦੀ ਇਜਾਜ਼ਤ ਦਿੰਦੇ ਹਨ ਜੋ ਪ੍ਰਤੀਰੋਧਕ ਪ੍ਰਤੀਰੋਧਕ ਪ੍ਰਤੀਕ੍ਰਿਆਵਾਂ ਦਾ ਕਾਰਨ ਬਣਦੇ ਹਨ, GVHD ਦੇ ਹੋਰ ਵਿਗਾੜ ਨੂੰ ਰੋਕ ਸਕਦੇ ਹਨ, ਅਤੇ ਸਰਜਰੀ ਐਸਕੋਰਟ ਤੋਂ ਬਾਅਦ ਹੈਪਲੋਡੈਂਟੀਕਲ HSCT ਵਾਲੇ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਇਮਿਊਨ ਫੰਕਸ਼ਨ ਨੂੰ ਬਹਾਲ ਕਰਦੇ ਹਨ।
(3) ਇਨਵੋਸਾ-ਕੇ
ਕੰਪਨੀ: TissueGene (KolonTissueGene) ਕੰਪਨੀ ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਜੁਲਾਈ 2017 ਵਿੱਚ ਦੱਖਣੀ ਕੋਰੀਆ ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਡੀਜਨਰੇਟਿਵ ਗੋਡੇ ਦੇ ਗਠੀਏ ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਇਨਵੋਸਾ-ਕੇ ਇੱਕ ਐਲੋਜੇਨਿਕ ਸੈੱਲ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜਿਸ ਵਿੱਚ ਮਨੁੱਖੀ ਕਾਂਡਰੋਸਾਈਟਸ ਸ਼ਾਮਲ ਹਨ।ਐਲੋਜੇਨਿਕ ਸੈੱਲਾਂ ਨੂੰ ਵਿਟਰੋ ਵਿੱਚ ਜੈਨੇਟਿਕ ਤੌਰ 'ਤੇ ਸੋਧਿਆ ਜਾਂਦਾ ਹੈ, ਅਤੇ ਸੰਸ਼ੋਧਿਤ ਸੈੱਲ ਇੰਟਰਾ-ਆਰਟੀਕੂਲਰ ਇੰਜੈਕਸ਼ਨ ਤੋਂ ਬਾਅਦ ਟਰਾਂਸਫਾਰਮਿੰਗ ਗ੍ਰੋਥ ਫੈਕਟਰ β1 (TGF-β1) ਨੂੰ ਪ੍ਰਗਟ ਕਰ ਸਕਦੇ ਹਨ ਅਤੇ ਛੁਪਾ ਸਕਦੇ ਹਨ।β1), ਜਿਸ ਨਾਲ ਗਠੀਏ ਦੇ ਲੱਛਣਾਂ ਵਿੱਚ ਸੁਧਾਰ ਹੁੰਦਾ ਹੈ।ਕਲੀਨਿਕਲ ਨਤੀਜੇ ਦਰਸਾਉਂਦੇ ਹਨ ਕਿ ਇਨਵੋਸਾ-ਕੇ ਗੋਡਿਆਂ ਦੇ ਗਠੀਏ ਵਿੱਚ ਮਹੱਤਵਪੂਰਨ ਸੁਧਾਰ ਕਰ ਸਕਦਾ ਹੈ।2019 ਵਿੱਚ ਦੱਖਣੀ ਕੋਰੀਆ ਦੇ ਡਰੱਗ ਰੈਗੂਲੇਟਰ ਦੁਆਰਾ ਲਾਇਸੈਂਸ ਨੂੰ ਰੱਦ ਕਰ ਦਿੱਤਾ ਗਿਆ ਸੀ ਕਿਉਂਕਿ ਨਿਰਮਾਤਾ ਨੇ ਵਰਤੀ ਗਈ ਸਮੱਗਰੀ ਨੂੰ ਗਲਤ ਢੰਗ ਨਾਲ ਲੇਬਲ ਕੀਤਾ ਸੀ।
(4) Zynteglo
ਕੰਪਨੀ: ਅਮਰੀਕੀ ਬਲੂਬਰਡ ਬਾਇਓ (ਬਲੂਬਰਡ ਬਾਇਓ) ਕੰਪਨੀ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਹੈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2019 ਵਿੱਚ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੁਆਰਾ ਪ੍ਰਵਾਨਿਤ, ਅਤੇ ਅਗਸਤ 2022 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਟ੍ਰਾਂਸਫਿਊਜ਼ਨ-ਨਿਰਭਰ β-ਥੈਲੇਸੀਮੀਆ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਜ਼ਿੰਟੇਗਲੋ ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਵਿੱਚ ਇੱਕ ਲੈਂਟੀਵਾਇਰਲ ਹੈ, ਜੋ ਮਰੀਜ਼ਾਂ ਤੋਂ ਹਟਾਏ ਗਏ ਹੇਮੇਟੋਪੋਇਟਿਕ ਸਟੈਮ ਸੈੱਲਾਂ ਵਿੱਚ ਸਧਾਰਣ β-ਗਲੋਬਿਨ ਜੀਨ (βA-T87Q-ਗਲੋਬਿਨ ਜੀਨ) ਦੀ ਕਾਰਜਸ਼ੀਲ ਕਾਪੀ ਨੂੰ ਪੇਸ਼ ਕਰਨ ਲਈ ਇੱਕ ਲੈਂਟੀਵਾਇਰਲ ਵੈਕਟਰ ਦੀ ਵਰਤੋਂ ਕਰਦਾ ਹੈ।, ਅਤੇ ਫਿਰ ਇਹਨਾਂ ਜੈਨੇਟਿਕ ਤੌਰ 'ਤੇ ਸੋਧੇ ਹੋਏ ਆਟੋਲੋਗਸ ਹੀਮੈਟੋਪੋਇਟਿਕ ਸਟੈਮ ਸੈੱਲਾਂ ਨੂੰ ਮਰੀਜ਼ ਵਿੱਚ ਵਾਪਸ ਪਾਓ।ਇੱਕ ਵਾਰ ਜਦੋਂ ਮਰੀਜ਼ ਕੋਲ ਇੱਕ ਆਮ βA-T87Q-ਗਲੋਬਿਨ ਜੀਨ ਹੁੰਦਾ ਹੈ, ਤਾਂ ਉਹ ਇੱਕ ਆਮ HbAT87Q ਪ੍ਰੋਟੀਨ ਪੈਦਾ ਕਰ ਸਕਦੇ ਹਨ, ਜੋ ਖੂਨ ਚੜ੍ਹਾਉਣ ਦੀ ਲੋੜ ਨੂੰ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਢੰਗ ਨਾਲ ਘਟਾ ਜਾਂ ਖਤਮ ਕਰ ਸਕਦਾ ਹੈ।ਇਹ ਇੱਕ ਵਾਰ ਦੀ ਥੈਰੇਪੀ ਹੈ ਜੋ 12 ਸਾਲ ਅਤੇ ਇਸ ਤੋਂ ਵੱਧ ਉਮਰ ਦੇ ਮਰੀਜ਼ਾਂ ਲਈ ਜੀਵਨ ਭਰ ਖੂਨ ਚੜ੍ਹਾਉਣ ਅਤੇ ਜੀਵਨ ਭਰ ਦਵਾਈਆਂ ਨੂੰ ਬਦਲਣ ਲਈ ਤਿਆਰ ਕੀਤੀ ਗਈ ਹੈ।
(5) ਸਕਾਈਸੋਨਾ
ਕੰਪਨੀ: ਅਮਰੀਕੀ ਬਲੂਬਰਡ ਬਾਇਓ (ਬਲੂਬਰਡ ਬਾਇਓ) ਕੰਪਨੀ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਹੈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਜੁਲਾਈ 2021 ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ EU ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਸ਼ੁਰੂਆਤੀ ਸੇਰੇਬ੍ਰਲ ਐਡਰੇਨੋਲੀਕੋਡੀਸਟ੍ਰੋਫੀ (CALD) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਸਕਾਈਸੋਨਾ ਜੀਨ ਥੈਰੇਪੀ ਸ਼ੁਰੂਆਤੀ ਸੇਰੇਬ੍ਰਲ ਐਡਰੇਨੋਲੀਕੋਡੀਸਟ੍ਰੋਫੀ (ਸੀਏਐਲਡੀ) ਦੇ ਇਲਾਜ ਲਈ ਪ੍ਰਵਾਨਿਤ ਇੱਕੋ-ਵਾਰ ਜੀਨ ਥੈਰੇਪੀ ਹੈ।ਸਕਾਈਸੋਨਾ (ਏਲੀਵਾਲਡੋਜੀਨ ਆਟੋਟੇਮਸੇਲ, ਲੈਂਟੀ-ਡੀ) ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਲੇਨਟੀ-ਡੀ ਵਿੱਚ ਇੱਕ ਹੇਮਾਟੋਪੋਇਟਿਕ ਸਟੈਮ ਸੈੱਲ ਲੈਨਟੀਵਾਇਰਲ ਹੈ।ਥੈਰੇਪੀ ਦੀ ਆਮ ਪ੍ਰਕਿਰਿਆ ਇਸ ਪ੍ਰਕਾਰ ਹੈ: ਆਟੋਲੋਗਸ ਹੈਮੇਟੋਪੋਇਟਿਕ ਸਟੈਮ ਸੈੱਲ ਮਰੀਜ਼ ਤੋਂ ਬਾਹਰ ਕੱਢੇ ਜਾਂਦੇ ਹਨ, ਮਨੁੱਖੀ ABCD1 ਜੀਨ ਨੂੰ ਲੈ ਕੇ ਲੈਂਟੀਵਾਇਰਸ ਦੁਆਰਾ ਵਿਟਰੋ ਵਿੱਚ ਸੋਧੇ ਜਾਂਦੇ ਹਨ, ਅਤੇ ਫਿਰ ਮਰੀਜ਼ ਵਿੱਚ ਵਾਪਸ ਪਾ ਦਿੱਤੇ ਜਾਂਦੇ ਹਨ।ABCD1 ਜੀਨ ਪਰਿਵਰਤਨ ਅਤੇ CALD ਨਾਲ 18 ਸਾਲ ਤੋਂ ਘੱਟ ਉਮਰ ਦੇ ਮਰੀਜ਼ਾਂ ਦੇ ਇਲਾਜ ਲਈ।
(6) ਕਿਮਰੀਆ
ਕੰਪਨੀ: ਨੋਵਾਰਟਿਸ ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਅਗਸਤ 2017 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਪ੍ਰੀਕਰਸਰ ਬੀ-ਸੈੱਲ ਐਕਿਊਟ ਲਿਮਫੋਬਲਾਸਟਿਕ ਲਿਊਕੇਮੀਆ (ALL) ਅਤੇ ਰੀਲੈਪਸਡ ਅਤੇ ਰਿਫ੍ਰੈਕਟਰੀ DLBCL ਦਾ ਇਲਾਜ।
ਟਿੱਪਣੀਆਂ: ਕਿਮਰੀਆ ਇੱਕ ਲੈਂਟੀਵਾਇਰਲ ਇਨ ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਡਰੱਗ ਹੈ, ਦੁਨੀਆ ਦੀ ਪਹਿਲੀ ਪ੍ਰਵਾਨਿਤ CAR-T ਥੈਰੇਪੀ, CD19 ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ ਅਤੇ ਸਹਿ-ਉਤੇਜਕ ਕਾਰਕ 4-1BB ਦੀ ਵਰਤੋਂ ਕਰਦੀ ਹੈ।ਅਮਰੀਕਾ ਵਿੱਚ ਕੀਮਤ $475,000 ਅਤੇ ਜਾਪਾਨ ਵਿੱਚ $313,000 ਹੈ।
(7) ਯੈਸਕਾਰਟਾ
ਕੰਪਨੀ: ਗਿਲਿਅਡ ਦੀ ਸਹਾਇਕ ਕੰਪਨੀ, Kite Pharma ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ ਹੈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਅਕਤੂਬਰ 2017 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਰੀਲੈਪਸਡ ਜਾਂ ਰਿਫ੍ਰੈਕਟਰੀ ਵੱਡੇ ਬੀ-ਸੈੱਲ ਲਿੰਫੋਮਾ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਯੈਸਕਾਰਟਾ ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਵਿੱਚ ਇੱਕ ਰੈਟਰੋਵਾਇਰਲ ਹੈ।ਇਹ ਦੁਨੀਆ ਵਿੱਚ ਪ੍ਰਵਾਨਿਤ ਦੂਜੀ CAR-T ਥੈਰੇਪੀ ਹੈ।ਇਹ CD19 ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦਾ ਹੈ ਅਤੇ CD28 ਦੇ ਕਾਸਟਿਮੂਲੇਟਰੀ ਫੈਕਟਰ ਦੀ ਵਰਤੋਂ ਕਰਦਾ ਹੈ।ਅਮਰੀਕਾ ਵਿੱਚ ਕੀਮਤ $373,000 ਹੈ।
(8) ਟੇਕਾਰਟਸ
ਕੰਪਨੀ: ਗਿਲਿਅਡ (GILD) ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: ਜੁਲਾਈ 2020 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਰੀਲੈਪਸਡ ਜਾਂ ਰਿਫ੍ਰੈਕਟਰੀ ਮੈਂਟਲ ਸੈੱਲ ਲਿਮਫੋਮਾ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਟੇਕਾਰਟਸ CD19 ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਣ ਵਾਲੀ ਇੱਕ ਆਟੋਲੋਗਸ CAR-T ਸੈੱਲ ਥੈਰੇਪੀ ਹੈ, ਅਤੇ ਦੁਨੀਆ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਪ੍ਰਵਾਨਿਤ ਤੀਜੀ CAR-T ਥੈਰੇਪੀ ਹੈ।
(9) ਬ੍ਰੇਅੰਜ਼ੀ
ਕੰਪਨੀ: ਬ੍ਰਿਸਟਲ-ਮਾਈਅਰਜ਼ ਸਕੁਇਬ (BMS) ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਫਰਵਰੀ 2021 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਰੀਲੈਪਸਡ ਜਾਂ ਰਿਫ੍ਰੈਕਟਰੀ (R/R) ਵੱਡੇ ਬੀ-ਸੈੱਲ ਲਿੰਫੋਮਾ (LBCL)।
ਟਿੱਪਣੀਆਂ: ਬ੍ਰੇਆਂਜ਼ੀ ਇੱਕ ਇਨ ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜੋ ਲੈਂਟੀਵਾਇਰਸ 'ਤੇ ਅਧਾਰਤ ਹੈ, ਅਤੇ ਚੌਥੀ CAR-T ਥੈਰੇਪੀ ਹੈ ਜੋ CD19 ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੇ ਹੋਏ, ਵਿਸ਼ਵ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰ ਹੈ।ਬ੍ਰਿਯਾਂਜ਼ੀ ਦੀ ਮਨਜ਼ੂਰੀ ਸੈਲੂਲਰ ਇਮਯੂਨੋਥੈਰੇਪੀ ਦੇ ਖੇਤਰ ਵਿੱਚ ਬ੍ਰਿਸਟਲ-ਮਾਈਅਰਜ਼ ਸਕੁਇਬ ਲਈ ਇੱਕ ਮੀਲ ਪੱਥਰ ਹੈ, ਜਿਸ ਨੂੰ ਬ੍ਰਿਸਟਲ-ਮਾਈਰਸ ਨੇ 2019 ਵਿੱਚ $74 ਬਿਲੀਅਨ ਵਿੱਚ ਸੇਲਜੀਨ ਨੂੰ ਹਾਸਲ ਕਰਨ ਵੇਲੇ ਹਾਸਲ ਕੀਤਾ ਸੀ।
(10) ਅਬੇਕਮਾ
ਕੰਪਨੀ: Bristol-Myers Squibb (BMS) ਅਤੇ ਬਲੂਬਰਡ ਬਾਇਓ ਦੁਆਰਾ ਸਹਿ-ਵਿਕਸਤ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਮਾਰਚ 2021 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਰੀਲੈਪਸਡ ਜਾਂ ਰਿਫ੍ਰੈਕਟਰੀ ਮਲਟੀਪਲ ਮਾਈਲੋਮਾ।
ਟਿੱਪਣੀਆਂ: ਅਬੇਕਮਾ ਇੱਕ ਲੈਂਟੀਵਾਇਰਸ-ਅਧਾਰਤ ਇਨ ਵਿਟਰੋ ਜੀਨ ਥੈਰੇਪੀ ਹੈ, ਵਿਸ਼ਵ ਦੀ ਪਹਿਲੀ CAR-T ਸੈੱਲ ਥੈਰੇਪੀ ਹੈ ਜੋ BCMA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ, ਅਤੇ FDA ਦੁਆਰਾ ਪ੍ਰਵਾਨਿਤ ਪੰਜਵੀਂ CAR-T ਥੈਰੇਪੀ ਹੈ।ਦਵਾਈ ਦਾ ਸਿਧਾਂਤ ਵਿਟਰੋ ਵਿੱਚ ਲੈਂਟੀਵਾਇਰਸ-ਵਿਚੋਲੇ ਜੈਨੇਟਿਕ ਸੋਧ ਦੁਆਰਾ ਮਰੀਜ਼ ਦੇ ਆਟੋਲੋਗਸ ਟੀ ਸੈੱਲਾਂ 'ਤੇ ਚਾਈਮੇਰਿਕ BCMA ਰੀਸੈਪਟਰ ਨੂੰ ਪ੍ਰਗਟ ਕਰਨਾ ਹੈ।ਸੈੱਲ ਜੀਨ ਡਰੱਗ ਦੇ ਨਿਵੇਸ਼ ਤੋਂ ਪਹਿਲਾਂ, ਮਰੀਜ਼ ਨੂੰ ਪੂਰਵ-ਇਲਾਜ ਲਈ ਸਾਈਕਲੋਫੋਸਫਾਮਾਈਡ ਅਤੇ ਫਲੂਡਾਰਾਬੀਨ ਦੇ ਦੋ ਮਿਸ਼ਰਣ ਪ੍ਰਾਪਤ ਹੋਏ।ਮਰੀਜ਼ ਤੋਂ ਅਣਸੋਧਿਤ ਟੀ ਸੈੱਲਾਂ ਨੂੰ ਹਟਾਉਣ ਲਈ ਇਲਾਜ, ਅਤੇ ਫਿਰ ਸੋਧੇ ਹੋਏ ਟੀ ਸੈੱਲਾਂ ਨੂੰ BCMA-ਪ੍ਰਗਟ ਕਰਨ ਵਾਲੇ ਕੈਂਸਰ ਸੈੱਲਾਂ ਨੂੰ ਲੱਭਣ ਅਤੇ ਮਾਰਨ ਲਈ ਮਰੀਜ਼ ਦੇ ਸਰੀਰ ਵਿੱਚ ਵਾਪਸ ਪਾਓ।
(11) ਲਿਬਮੇਲਡੀ
ਕੰਪਨੀ: Orchard Therapeutics ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਦਸੰਬਰ 2020 ਵਿੱਚ ਸੂਚੀਬੱਧ ਕਰਨ ਲਈ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਮੈਟਾਕਰੋਮੈਟਿਕ ਲਿਊਕੋਡੀਸਟ੍ਰੋਫੀ (ਐਮਐਲਡੀ) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਲਿਬਮੇਲਡੀ ਇੱਕ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜੋ ਆਟੋਲੋਗਸ CD34+ ਸੈੱਲਾਂ ਦੇ ਵਿਟਰੋ ਜੀਨ ਸੋਧ ਵਿੱਚ ਲੈਂਟੀਵਾਇਰਲ 'ਤੇ ਅਧਾਰਤ ਹੈ।ਕਲੀਨਿਕਲ ਡੇਟਾ ਦਰਸਾਉਂਦੇ ਹਨ ਕਿ ਲਿਬਮੇਲਡੀ ਦਾ ਇੱਕ ਸਿੰਗਲ ਇਨਫਿਊਜ਼ਨ ਇਨਫਿਊਜ਼ਨ ਉਸੇ ਉਮਰ ਦੇ ਇਲਾਜ ਨਾ ਕੀਤੇ ਗਏ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਸ਼ੁਰੂਆਤੀ ਸ਼ੁਰੂਆਤੀ ਐਮਐਲਡੀ ਅਤੇ ਗੰਭੀਰ ਮੋਟਰ ਅਤੇ ਬੋਧਾਤਮਕ ਕਮਜ਼ੋਰੀ ਦੇ ਕੋਰਸ ਨੂੰ ਸੋਧਣ ਵਿੱਚ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਹੈ।
(12) ਬੇਨੋਦਾ
ਕੰਪਨੀ: WuXi Junuo ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਸਤੰਬਰ 2021 ਵਿੱਚ NMPA ਦੁਆਰਾ ਅਧਿਕਾਰਤ ਤੌਰ 'ਤੇ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਦੂਜੀ-ਲਾਈਨ ਜਾਂ ਵਧੇਰੇ ਪ੍ਰਣਾਲੀਗਤ ਥੈਰੇਪੀ ਤੋਂ ਬਾਅਦ ਬਾਲਗ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਰੀਲੈਪਸਡ ਜਾਂ ਰਿਫ੍ਰੈਕਟਰੀ ਵੱਡੇ ਬੀ-ਸੈੱਲ ਲਿੰਫੋਮਾ (r/r LBCL) ਦਾ ਇਲਾਜ।
ਟਿੱਪਣੀਆਂ: ਬੇਨੋਡਾ ਇੱਕ ਐਂਟੀ-CD19 CAR-T ਜੀਨ ਥੈਰੇਪੀ ਹੈ, ਅਤੇ ਇਹ WuXi Junuo ਦਾ ਮੁੱਖ ਉਤਪਾਦ ਵੀ ਹੈ।ਇਹ ਚੀਨ ਵਿੱਚ ਪ੍ਰਵਾਨਿਤ ਦੂਜਾ CAR-T ਉਤਪਾਦ ਹੈ, ਰੀਲੈਪਸਡ/ਰਿਫ੍ਰੈਕਟਰੀ ਵੱਡੇ ਬੀ-ਸੈੱਲ ਲਿੰਫੋਮਾ ਨੂੰ ਛੱਡ ਕੇ।ਇਸ ਤੋਂ ਇਲਾਵਾ, ਵੂਕਸੀ ਜੂਨੂਓ ਨੇ ਕਈ ਹੋਰ ਸੰਕੇਤਾਂ ਦੇ ਇਲਾਜ ਲਈ ਰੁਈਕੀ ਓਰੇਂਜ਼ਾ ਇੰਜੈਕਸ਼ਨ ਵਿਕਸਿਤ ਕਰਨ ਦੀ ਵੀ ਯੋਜਨਾ ਬਣਾਈ ਹੈ, ਜਿਸ ਵਿੱਚ ਫੋਲੀਕੂਲਰ ਲਿਮਫੋਮਾ (FL), ਮੈਂਟਲ ਸੈੱਲ ਲਿਮਫੋਮਾ (MCL), ਕ੍ਰੋਨਿਕ ਲਿਮਫੋਸਾਈਟਿਕ ਲਿਊਕੇਮੀਆ (CLL), ਸੈਕਿੰਡ-ਲਾਈਨ ਡਿਫਿਊਜ਼ ਲਾਰਜ ਬੀ-ਸੈੱਲ ਲਿਮਫੋਮਾ (ਏ.ਐੱਲ.ਡੀ.ਐੱਲ.ਐੱਲ.ਯੂ.ਐਕਸ.ਐੱਲ.ਐੱਲ.ਯੂ.
(13) ਕਾਰਵਿਕਟੀ
ਕੰਪਨੀ: Legend Bio ਦਾ ਪਹਿਲਾ ਪ੍ਰਵਾਨਿਤ ਉਤਪਾਦ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਫਰਵਰੀ 2022 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਰੀਲੈਪਸਡ ਜਾਂ ਰਿਫ੍ਰੈਕਟਰੀ ਮਲਟੀਪਲ ਮਾਈਲੋਮਾ (R/R MM) ਦਾ ਇਲਾਜ।
ਟਿੱਪਣੀਆਂ: CARVYKTI (ciltacabtagene autoleucel, ਜਿਸਨੂੰ Cilta-cel ਕਿਹਾ ਜਾਂਦਾ ਹੈ) ਇੱਕ CAR-T ਸੈੱਲ ਇਮਿਊਨ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜਿਸ ਵਿੱਚ B ਸੈੱਲ ਪਰਿਪੱਕਤਾ ਐਂਟੀਜੇਨ (BCMA) ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਣ ਵਾਲੇ ਦੋ ਸਿੰਗਲ-ਡੋਮੇਨ ਐਂਟੀਬਾਡੀਜ਼ ਹਨ।ਡੇਟਾ ਦਰਸਾਉਂਦਾ ਹੈ ਕਿ CARVYKTI ਨੇ ਰੀਲੈਪਸਡ ਜਾਂ ਰੀਫ੍ਰੈਕਟਰੀ ਮਲਟੀਪਲ ਮਾਈਲੋਮਾ ਵਾਲੇ ਮਰੀਜ਼ਾਂ ਵਿੱਚ 98% ਤੱਕ ਦੀ ਸਮੁੱਚੀ ਪ੍ਰਤੀਕਿਰਿਆ ਦਰ ਦਾ ਪ੍ਰਦਰਸ਼ਨ ਕੀਤਾ ਜਿਨ੍ਹਾਂ ਨੇ ਚਾਰ ਜਾਂ ਵੱਧ ਪਹਿਲਾਂ ਇਲਾਜ ਪ੍ਰਾਪਤ ਕੀਤੇ ਸਨ, ਜਿਸ ਵਿੱਚ ਪ੍ਰੋਟੀਸੋਮ ਇਨਿਹਿਬਟਰਸ, ਇਮਯੂਨੋਮੋਡਿਊਲਟਰ, ਅਤੇ ਐਂਟੀ-CD38 ਮੋਨੋਕਲੋਨਲ ਐਂਟੀਬਾਡੀਜ਼ ਸ਼ਾਮਲ ਹਨ।
2. ਵਾਇਰਲ ਵੈਕਟਰਾਂ 'ਤੇ ਅਧਾਰਤ ਵੀਵੋ ਜੀਨ ਥੈਰੇਪੀ ਵਿੱਚ
(1) ਜੈਨਡੀਸੀਨ / ਦੁਬਾਰਾ ਜਨਮ ਲੈਣਾ
ਕੰਪਨੀ: ਸ਼ੇਨਜ਼ੇਨ ਸਾਈਬੈਨੂਓ ਕੰਪਨੀ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2003 ਵਿੱਚ ਚੀਨ ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਸਿਰ ਅਤੇ ਗਰਦਨ ਦੇ ਸਕਵਾਮਸ ਸੈੱਲ ਕਾਰਸਿਨੋਮਾ ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਰੀਕੌਂਬੀਨੈਂਟ ਹਿਊਮਨ p53 ਐਡੀਨੋਵਾਇਰਸ ਇੰਜੈਕਸ਼ਨ ਗੈਂਡੀਸੀਨ/ਜਿਨਸ਼ੇਂਗਸ਼ੇਂਗ ਸ਼ੇਨਜ਼ੇਨ ਸਾਈਬੈਨੂਓ ਕੰਪਨੀ ਦੀ ਮਲਕੀਅਤ ਵਾਲੇ ਸੁਤੰਤਰ ਬੌਧਿਕ ਸੰਪੱਤੀ ਅਧਿਕਾਰਾਂ ਵਾਲੀ ਇੱਕ ਐਡੀਨੋਵਾਇਰਸ ਵੈਕਟਰ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈ ਹੈ।ਡਰੱਗ ਆਮ ਮਨੁੱਖੀ ਟਿਊਮਰ ਨੂੰ ਦਬਾਉਣ ਵਾਲੇ ਜੀਨ p53 ਅਤੇ ਨਕਲੀ ਤੌਰ 'ਤੇ ਸੰਸ਼ੋਧਿਤ ਰੀਕੌਂਬੀਨੈਂਟ ਪ੍ਰਤੀਕ੍ਰਿਤੀ-ਘਾਟ ਮਨੁੱਖੀ ਐਡੀਨੋਵਾਇਰਸ ਟਾਈਪ 5 ਦੀ ਬਣੀ ਹੋਈ ਹੈ। ਸਾਬਕਾ ਐਂਟੀ-ਟਿਊਮਰ ਪ੍ਰਭਾਵ ਨੂੰ ਲਾਗੂ ਕਰਨ ਲਈ ਡਰੱਗ ਦਾ ਮੁੱਖ ਢਾਂਚਾ ਹੈ, ਅਤੇ ਬਾਅਦ ਵਾਲਾ ਮੁੱਖ ਤੌਰ 'ਤੇ ਕੈਰੀਰੀ ਵਜੋਂ ਕੰਮ ਕਰਦਾ ਹੈ।ਐਡੀਨੋਵਾਇਰਸ ਵੈਕਟਰ ਉਪਚਾਰਕ ਜੀਨ p53 ਨੂੰ ਟੀਚੇ ਦੇ ਸੈੱਲ ਵਿੱਚ ਲੈ ਜਾਂਦਾ ਹੈ, ਅਤੇ ਟੀਚਾ ਸੈੱਲ ਵਿੱਚ ਟਿਊਮਰ ਨੂੰ ਦਬਾਉਣ ਵਾਲੇ ਜੀਨ p53 ਨੂੰ ਪ੍ਰਗਟ ਕਰਦਾ ਹੈ।ਉਤਪਾਦ ਵੱਖ-ਵੱਖ ਕੈਂਸਰ ਵਿਰੋਧੀ ਜੀਨਾਂ ਨੂੰ ਨਿਯੰਤ੍ਰਿਤ ਕਰ ਸਕਦਾ ਹੈ ਅਤੇ ਵੱਖ-ਵੱਖ ਆਨਕੋਜੀਨਾਂ ਦੀਆਂ ਗਤੀਵਿਧੀਆਂ ਨੂੰ ਨਿਯੰਤ੍ਰਿਤ ਕਰ ਸਕਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਸਰੀਰ ਦੇ ਟਿਊਮਰ ਵਿਰੋਧੀ ਪ੍ਰਭਾਵ ਨੂੰ ਵਧਾਇਆ ਜਾ ਸਕਦਾ ਹੈ ਅਤੇ ਟਿਊਮਰਾਂ ਨੂੰ ਮਾਰਨ ਦੇ ਉਦੇਸ਼ ਨੂੰ ਪ੍ਰਾਪਤ ਕੀਤਾ ਜਾ ਸਕਦਾ ਹੈ।
(2) ਰਿਗਵੀਰ
ਕੰਪਨੀ: ਲਾਤਵੀਅਨ ਕੰਪਨੀ ਲਾਤੀਮਾ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: 2004 ਵਿੱਚ ਲਾਤਵੀਆ ਵਿੱਚ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਮੇਲੇਨੋਮਾ ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਰਿਗਵੀਰ ਇੱਕ ਜੀਨ-ਸੰਸ਼ੋਧਿਤ ECHO-7 ਐਂਟਰੋਵਾਇਰਸ ਵੈਕਟਰ 'ਤੇ ਅਧਾਰਤ ਇੱਕ ਜੀਨ ਥੈਰੇਪੀ ਹੈ, ਜਿਸਦੀ ਵਰਤੋਂ ਲਾਤਵੀਆ, ਐਸਟੋਨੀਆ, ਪੋਲੈਂਡ, ਅਰਮੀਨੀਆ, ਬੇਲਾਰੂਸ ਅਤੇ ਹੋਰ ਸਥਾਨਾਂ ਵਿੱਚ ਕੀਤੀ ਗਈ ਹੈ, ਅਤੇ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੇ EMA ਨਾਲ ਵੀ ਰਜਿਸਟਰ ਕੀਤਾ ਜਾ ਰਿਹਾ ਹੈ।.ਪਿਛਲੇ ਦਸ ਸਾਲਾਂ ਦੇ ਕਲੀਨਿਕਲ ਕੇਸਾਂ ਨੇ ਸਾਬਤ ਕੀਤਾ ਹੈ ਕਿ ਰਿਗਵੀਰ ਓਨਕੋਲੀਟਿਕ ਵਾਇਰਸ ਸੁਰੱਖਿਅਤ ਅਤੇ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਹੈ, ਅਤੇ ਮੇਲਾਨੋਮਾ ਦੇ ਮਰੀਜ਼ਾਂ ਦੀ ਬਚਣ ਦੀ ਦਰ ਨੂੰ 4-6 ਗੁਣਾ ਤੱਕ ਸੁਧਾਰ ਸਕਦਾ ਹੈ।ਇਸ ਤੋਂ ਇਲਾਵਾ, ਇਹ ਥੈਰੇਪੀ ਕੋਲੋਰੈਕਟਲ ਕੈਂਸਰ, ਪੈਨਕ੍ਰੀਆਟਿਕ ਕੈਂਸਰ, ਬਲੈਡਰ ਕੈਂਸਰ ਸਮੇਤ ਕਈ ਤਰ੍ਹਾਂ ਦੇ ਹੋਰ ਕੈਂਸਰਾਂ ਲਈ ਵੀ ਢੁਕਵੀਂ ਹੈ।ਕੈਂਸਰ, ਗੁਰਦੇ ਦਾ ਕੈਂਸਰ, ਪ੍ਰੋਸਟੇਟ ਕੈਂਸਰ, ਫੇਫੜਿਆਂ ਦਾ ਕੈਂਸਰ, ਗਰੱਭਾਸ਼ਯ ਕੈਂਸਰ, ਲਿਮਫੋਸਾਰਕੋਮਾ, ਆਦਿ।
(3) ਓਨਕੋਰੀਨ/ਅੰਕੇਰੂਈ
ਕੰਪਨੀ: ਸ਼ੰਘਾਈ ਸਨਵੇ ਬਾਇਓਟੈਕਨਾਲੋਜੀ ਕੰਪਨੀ, ਲਿਮਿਟੇਡ ਦੁਆਰਾ ਵਿਕਸਤ
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2005 ਵਿੱਚ ਚੀਨ ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਸਿਰ ਅਤੇ ਗਰਦਨ ਦੇ ਟਿਊਮਰ, ਜਿਗਰ ਦਾ ਕੈਂਸਰ, ਪੈਨਕ੍ਰੀਆਟਿਕ ਕੈਂਸਰ, ਸਰਵਾਈਕਲ ਕੈਂਸਰ ਅਤੇ ਹੋਰ ਕੈਂਸਰਾਂ ਦਾ ਇਲਾਜ।
ਟਿੱਪਣੀਆਂ: ਓਨਕੋਰੀਨ ਇੱਕ ਵੈਕਟਰ ਦੇ ਤੌਰ ਤੇ ਐਡੀਨੋਵਾਇਰਸ ਦੀ ਵਰਤੋਂ ਕਰਨ ਵਾਲਾ ਇੱਕ ਓਨਕੋਲੀਟਿਕ ਵਾਇਰਸ ਜੀਨ ਥੈਰੇਪੀ ਉਤਪਾਦ ਹੈ।ਪ੍ਰਾਪਤ ਕੀਤਾ ਓਨਕੋਲੀਟਿਕ ਐਡੀਨੋਵਾਇਰਸ ਖਾਸ ਤੌਰ 'ਤੇ ਟਿਊਮਰ ਦੀ ਘਾਟ ਜਾਂ ਅਸਧਾਰਨ p53 ਜੀਨ ਵਿੱਚ ਦੁਹਰ ਸਕਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਟਿਊਮਰ ਸੈੱਲ ਲਾਈਸਿਸ ਹੋ ਸਕਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਟਿਊਮਰ ਸੈੱਲਾਂ ਨੂੰ ਮਾਰਿਆ ਜਾ ਸਕਦਾ ਹੈ।ਆਮ ਸੈੱਲਾਂ ਨੂੰ ਨੁਕਸਾਨ ਪਹੁੰਚਾਏ ਬਿਨਾਂ।ਕਲੀਨਿਕਲ ਨਤੀਜੇ ਦਰਸਾਉਂਦੇ ਹਨ ਕਿ ਐਂਕੇ ਰੁਈ ਵਿੱਚ ਕਈ ਕਿਸਮ ਦੇ ਘਾਤਕ ਟਿਊਮਰ ਲਈ ਚੰਗੀ ਸੁਰੱਖਿਆ ਅਤੇ ਪ੍ਰਭਾਵ ਹੈ।
(4) ਗਲਾਈਬੇਰਾ
ਕੰਪਨੀ: ਯੂਨੀਕਿਊਰ ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2012 ਵਿੱਚ ਯੂਰਪ ਵਿੱਚ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਸਖਤੀ ਨਾਲ ਸੀਮਤ ਚਰਬੀ ਵਾਲੀ ਖੁਰਾਕ ਦੇ ਬਾਵਜੂਦ ਪੈਨਕ੍ਰੇਟਾਈਟਸ ਦੇ ਗੰਭੀਰ ਜਾਂ ਆਵਰਤੀ ਐਪੀਸੋਡਾਂ ਦੇ ਨਾਲ ਲਿਪੋਪ੍ਰੋਟੀਨ ਲਿਪੇਸ ਦੀ ਘਾਟ (LPLD) ਦਾ ਇਲਾਜ।
ਟਿੱਪਣੀਆਂ: ਗਲਾਈਬੇਰਾ (ਐਲਿਪੋਜੀਨ ਟਿਪਰਵੋਵੇਕ) ਇੱਕ ਵੈਕਟਰ ਦੇ ਤੌਰ ਤੇ ਏਏਵੀ 'ਤੇ ਅਧਾਰਤ ਇੱਕ ਜੀਨ ਥੈਰੇਪੀ ਡਰੱਗ ਹੈ।ਇਹ ਥੈਰੇਪੀ ਮਾਸਪੇਸ਼ੀ ਸੈੱਲਾਂ ਵਿੱਚ ਉਪਚਾਰਕ ਜੀਨ ਐਲਪੀਐਲ ਨੂੰ ਟ੍ਰਾਂਸਫਰ ਕਰਨ ਲਈ ਇੱਕ ਵੈਕਟਰ ਦੇ ਤੌਰ ਤੇ ਏਏਵੀ ਦੀ ਵਰਤੋਂ ਕਰਦੀ ਹੈ, ਤਾਂ ਜੋ ਸੰਬੰਧਿਤ ਸੈੱਲ ਇੱਕ ਨਿਸ਼ਚਿਤ ਮਾਤਰਾ ਵਿੱਚ ਲਿਪੋਪ੍ਰੋਟੀਨ ਲਿਪੇਸ ਪੈਦਾ ਕਰ ਸਕਣ, ਇਹ ਬਿਮਾਰੀ ਤੋਂ ਛੁਟਕਾਰਾ ਪਾਉਣ ਵਿੱਚ ਭੂਮਿਕਾ ਨਿਭਾਉਂਦਾ ਹੈ, ਅਤੇ ਇਹ ਥੈਰੇਪੀ ਇੱਕ ਪ੍ਰਸ਼ਾਸਨ ਤੋਂ ਬਾਅਦ ਲੰਬੇ ਸਮੇਂ ਤੱਕ ਪ੍ਰਭਾਵੀ ਹੁੰਦੀ ਹੈ (ਪ੍ਰਭਾਵ ਕਈ ਸਾਲਾਂ ਤੱਕ ਰਹਿ ਸਕਦਾ ਹੈ)।ਡਰੱਗ ਨੂੰ 2017 ਵਿੱਚ ਸੂਚੀਬੱਧ ਕੀਤਾ ਗਿਆ ਸੀ, ਅਤੇ ਇਸਦੀ ਸੂਚੀਬੱਧ ਕਰਨ ਦੇ ਕਾਰਨ ਦੋ ਕਾਰਕਾਂ ਨਾਲ ਸਬੰਧਤ ਹੋ ਸਕਦੇ ਹਨ: ਬਹੁਤ ਜ਼ਿਆਦਾ ਕੀਮਤ ਅਤੇ ਸੀਮਤ ਬਾਜ਼ਾਰ ਦੀ ਮੰਗ।ਦਵਾਈ ਦੇ ਇੱਕ ਸਿੰਗਲ ਇਲਾਜ ਦੀ ਔਸਤ ਕੀਮਤ 1 ਮਿਲੀਅਨ ਅਮਰੀਕੀ ਡਾਲਰ ਹੈ, ਅਤੇ ਹੁਣ ਤੱਕ ਸਿਰਫ ਇੱਕ ਮਰੀਜ਼ ਨੇ ਇਸਨੂੰ ਖਰੀਦਿਆ ਅਤੇ ਵਰਤਿਆ ਹੈ।ਹਾਲਾਂਕਿ ਮੈਡੀਕਲ ਇੰਸ਼ੋਰੈਂਸ ਕੰਪਨੀ ਨੇ ਇਸਦੀ 900,000 ਅਮਰੀਕੀ ਡਾਲਰਾਂ ਦੀ ਭਰਪਾਈ ਕੀਤੀ, ਪਰ ਇਹ ਬੀਮਾ ਕੰਪਨੀ ਲਈ ਵੀ ਇੱਕ ਵੱਡਾ ਬੋਝ ਹੈ।ਇਸ ਤੋਂ ਇਲਾਵਾ, ਡਰੱਗ ਲਈ ਸੰਕੇਤ ਬਹੁਤ ਦੁਰਲੱਭ ਹਨ, 1 ਮਿਲੀਅਨ ਵਿੱਚੋਂ 1 ਦੀ ਘਟਨਾ ਦਰ ਅਤੇ ਗਲਤ ਨਿਦਾਨ ਦੀ ਉੱਚ ਦਰ ਦੇ ਨਾਲ।
(5) ਇਮਲੀਜਿਕ
ਕੰਪਨੀ: ਐਮਜੇਨ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2015 ਵਿੱਚ, ਇਸਨੂੰ ਸੰਯੁਕਤ ਰਾਜ ਅਤੇ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਵਿੱਚ ਸੂਚੀਬੱਧ ਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ ਸੀ।
ਸੰਕੇਤ: ਮੇਲਾਨੋਮਾ ਜਖਮਾਂ ਦਾ ਇਲਾਜ ਜੋ ਸਰਜਰੀ ਦੁਆਰਾ ਪੂਰੀ ਤਰ੍ਹਾਂ ਨਹੀਂ ਹਟਾਇਆ ਜਾ ਸਕਦਾ।
ਟਿੱਪਣੀਆਂ: ਇਮਲੀਜਿਕ ਇੱਕ ਜੈਨੇਟਿਕ ਤੌਰ 'ਤੇ ਸੋਧਿਆ ਗਿਆ ਹੈ (ਇਸਦੇ ICP34.5 ਅਤੇ ICP47 ਜੀਨ ਦੇ ਟੁਕੜਿਆਂ ਨੂੰ ਮਿਟਾਉਣਾ, ਅਤੇ ਮਨੁੱਖੀ ਗ੍ਰੈਨਿਊਲੋਸਾਈਟ-ਮੈਕ੍ਰੋਫੇਜ ਕਲੋਨੀ-ਸਟਿਮੂਲੇਟਿੰਗ ਫੈਕਟਰ GM-CSF ਜੀਨ ਨੂੰ ਵਾਇਰਸ ਵਿੱਚ ਸ਼ਾਮਲ ਕਰਨਾ) ਐਟੇਨਿਊਏਟਿਡ ਹਰਪੀਸ ਸਿੰਪਲੈਕਸ ਵਾਇਰਸ ਟਾਈਪ 1 (ਐਚਐਸਵੀ-ਡੀਏ-ਐਪ ਵਾਇਰਸ, ਐੱਫ.ਐੱਸ.ਵੀ.-ਡੀ.ਏ.ਐਪ., ਐੱਫ.ਐੱਚ.ਐੱਸ.ਵੀ.-ਏ.ਪੀ. ਐੱਫ. .ਪ੍ਰਸ਼ਾਸਨ ਦਾ ਤਰੀਕਾ ਇੰਟਰਾਲੇਸਨਲ ਇੰਜੈਕਸ਼ਨ ਹੈ.ਮੇਲਾਨੋਮਾ ਦੇ ਜਖਮਾਂ ਵਿੱਚ ਸਿੱਧਾ ਟੀਕਾ ਟਿਊਮਰ ਸੈੱਲਾਂ ਦੇ ਫਟਣ ਦਾ ਕਾਰਨ ਬਣ ਸਕਦਾ ਹੈ ਅਤੇ ਟਿਊਮਰ-ਵਿਰੋਧੀ ਪ੍ਰਤੀਰੋਧਕ ਪ੍ਰਤੀਕ੍ਰਿਆਵਾਂ ਨੂੰ ਉਤਸ਼ਾਹਿਤ ਕਰਨ ਲਈ ਟਿਊਮਰ-ਪ੍ਰਾਪਤ ਐਂਟੀਜੇਨਜ਼ ਅਤੇ GM-CSF ਛੱਡ ਸਕਦਾ ਹੈ।
(6) Luxturna
ਕੰਪਨੀ: ਸਪਾਰਕ ਥੈਰੇਪਿਊਟਿਕਸ ਦੁਆਰਾ ਵਿਕਸਤ, ਇੱਕ ਰੋਚ ਸਹਾਇਕ ਕੰਪਨੀ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2017 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ, ਅਤੇ ਫਿਰ 2018 ਵਿੱਚ ਯੂਰਪ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: RPE65 ਜੀਨ ਦੀ ਦੋਹਰੀ ਕਾਪੀ ਵਿਚ ਪਰਿਵਰਤਨਸ਼ੀਲ ਰੈਟਿਨਲ ਸੈੱਲਾਂ ਦੀ ਕਾਫੀ ਸੰਖਿਆ ਦੇ ਨਾਲ ਪਰਿਵਰਤਨ ਦੇ ਕਾਰਨ ਨਜ਼ਰ ਦੇ ਨੁਕਸਾਨ ਵਾਲੇ ਬੱਚਿਆਂ ਅਤੇ ਬਾਲਗਾਂ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: Luxturna ਇੱਕ AAV- ਅਧਾਰਤ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜੋ ਸਬਰੇਟੀਨਲ ਇੰਜੈਕਸ਼ਨ ਦੁਆਰਾ ਚਲਾਈ ਜਾਂਦੀ ਹੈ।ਜੀਨ ਥੈਰੇਪੀ ਮਰੀਜ਼ ਦੇ ਰੈਟਿਨਲ ਸੈੱਲਾਂ ਵਿੱਚ ਆਮ RPE65 ਜੀਨ ਦੀ ਇੱਕ ਕਾਰਜਸ਼ੀਲ ਕਾਪੀ ਨੂੰ ਪੇਸ਼ ਕਰਨ ਲਈ ਇੱਕ ਕੈਰੀਅਰ ਵਜੋਂ AAV2 ਦੀ ਵਰਤੋਂ ਕਰਦੀ ਹੈ, ਤਾਂ ਜੋ ਸੰਬੰਧਿਤ ਸੈੱਲ ਮਰੀਜ਼ ਦੇ RPE65 ਪ੍ਰੋਟੀਨ ਦੇ ਨੁਕਸ ਦੀ ਭਰਪਾਈ ਕਰਨ ਲਈ ਆਮ RPE65 ਪ੍ਰੋਟੀਨ ਨੂੰ ਪ੍ਰਗਟ ਕਰਦੇ ਹਨ, ਜਿਸ ਨਾਲ ਮਰੀਜ਼ ਦੀ ਨਜ਼ਰ ਵਿੱਚ ਸੁਧਾਰ ਹੁੰਦਾ ਹੈ।
(7) ਜ਼ੋਲਗਨਸਮਾ
ਕੰਪਨੀ: AveXis ਦੁਆਰਾ ਵਿਕਸਤ, Novartis ਦੀ ਇੱਕ ਸਹਾਇਕ ਕੰਪਨੀ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਮਈ 2019 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਸਪਾਈਨਲ ਮਾਸਕੂਲਰ ਐਟ੍ਰੋਫੀ (ਸਪਾਈਨਲ ਮਾਸਕੂਲਰ ਐਟ੍ਰੋਫੀ, ਐਸਐਮਏ) 2 ਸਾਲ ਤੋਂ ਘੱਟ ਉਮਰ ਦੇ ਮਰੀਜ਼ਾਂ ਦਾ ਇਲਾਜ।
ਟਿੱਪਣੀਆਂ: ਜ਼ੋਲਗਨਸਮਾ ਏਏਵੀ ਵੈਕਟਰ 'ਤੇ ਅਧਾਰਤ ਇੱਕ ਜੀਨ ਥੈਰੇਪੀ ਹੈ।ਇਹ ਦਵਾਈ ਸਪਾਈਨਲ ਮਾਸਕੂਲਰ ਐਟ੍ਰੋਫੀ ਲਈ ਵਿਸ਼ਵ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਪ੍ਰਵਾਨਿਤ ਇੱਕ-ਵਾਰ ਇਲਾਜ ਯੋਜਨਾ ਹੈ।ਪੰਨਾ, ਇੱਕ ਮੀਲ ਪੱਥਰ ਤਰੱਕੀ ਹੈ।ਇਹ ਜੀਨ ਥੈਰੇਪੀ scAAV9 ਵੈਕਟਰ ਦੀ ਵਰਤੋਂ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਆਮ SMN1 ਜੀਨ ਨੂੰ ਨਾੜੀ ਨਿਵੇਸ਼ ਦੁਆਰਾ ਪੇਸ਼ ਕਰਨ ਲਈ ਕਰਦੀ ਹੈ, ਆਮ SMN1 ਪ੍ਰੋਟੀਨ ਪੈਦਾ ਕਰਦੀ ਹੈ, ਜਿਸ ਨਾਲ ਪ੍ਰਭਾਵਿਤ ਸੈੱਲਾਂ ਜਿਵੇਂ ਕਿ ਮੋਟਰ ਨਿਊਰੋਨਸ ਦੇ ਕੰਮ ਵਿੱਚ ਸੁਧਾਰ ਹੁੰਦਾ ਹੈ।ਇਸ ਦੇ ਉਲਟ, SMA ਦਵਾਈਆਂ ਸਪਿਨਰਾਜ਼ਾ ਅਤੇ ਐਵਰੀਸਡੀ ਨੂੰ ਲੰਬੇ ਸਮੇਂ ਲਈ ਦੁਹਰਾਉਣ ਦੀ ਲੋੜ ਹੁੰਦੀ ਹੈ, ਸਪਿਨਰਾਜ਼ਾ ਨੂੰ ਹਰ ਚਾਰ ਮਹੀਨਿਆਂ ਵਿੱਚ ਰੀੜ੍ਹ ਦੀ ਹੱਡੀ ਦੇ ਇੰਜੈਕਸ਼ਨ ਦੇ ਰੂਪ ਵਿੱਚ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ, ਅਤੇ Evrysdi, ਇੱਕ ਰੋਜ਼ਾਨਾ ਮੂੰਹ ਦੀ ਦਵਾਈ।
(8) ਡੈਲੀਟੈਕਟ
ਕੰਪਨੀ: ਦਾਈਚੀ ਸਾਂਕਯੋ ਕੰਪਨੀ ਲਿਮਿਟੇਡ (TYO: 4568) ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: ਜੂਨ 2021 ਵਿੱਚ ਜਾਪਾਨੀ ਸਿਹਤ, ਕਿਰਤ ਅਤੇ ਭਲਾਈ ਮੰਤਰਾਲੇ (MHLW) ਤੋਂ ਸ਼ਰਤੀਆ ਪ੍ਰਵਾਨਗੀ।
ਸੰਕੇਤ: ਘਾਤਕ ਗਲੀਓਮਾ ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਡੇਲੀਟੈਕਟ ਚੌਥਾ ਓਨਕੋਲੀਟਿਕ ਵਾਇਰਸ ਜੀਨ ਥੈਰੇਪੀ ਉਤਪਾਦ ਹੈ ਜੋ ਵਿਸ਼ਵ ਪੱਧਰ 'ਤੇ ਪ੍ਰਵਾਨਿਤ ਹੈ ਅਤੇ ਘਾਤਕ ਗਲਾਈਓਮਾ ਦੇ ਇਲਾਜ ਲਈ ਪ੍ਰਵਾਨਿਤ ਪਹਿਲਾ ਓਨਕੋਲੀਟਿਕ ਵਾਇਰਸ ਉਤਪਾਦ ਹੈ।ਡੇਲੀਟੈਕਟ ਇੱਕ ਜੈਨੇਟਿਕ ਤੌਰ 'ਤੇ ਇੰਜਨੀਅਰਡ ਹਰਪੀਜ਼ ਸਿੰਪਲੈਕਸ ਵਾਇਰਸ ਟਾਈਪ 1 (HSV-1) ਓਨਕੋਲੀਟਿਕ ਵਾਇਰਸ ਹੈ ਜੋ ਡਾ. ਟੋਡੋ ਅਤੇ ਸਹਿਯੋਗੀਆਂ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਹੈ।ਡੈਲੀਟੈਕਟ ਦੂਜੀ ਪੀੜ੍ਹੀ ਦੇ HSV-1 ਦੇ G207 ਜੀਨੋਮ ਵਿੱਚ ਇੱਕ ਵਾਧੂ ਮਿਟਾਉਣ ਵਾਲੇ ਪਰਿਵਰਤਨ ਨੂੰ ਪੇਸ਼ ਕਰਦਾ ਹੈ, ਇੱਕ ਉੱਚ ਸੁਰੱਖਿਆ ਪ੍ਰੋਫਾਈਲ ਨੂੰ ਕਾਇਮ ਰੱਖਦੇ ਹੋਏ, ਕੈਂਸਰ ਸੈੱਲਾਂ ਵਿੱਚ ਇਸਦੇ ਚੋਣਵੇਂ ਪ੍ਰਤੀਕ੍ਰਿਤੀ ਨੂੰ ਵਧਾਉਂਦਾ ਹੈ ਅਤੇ ਐਂਟੀ-ਟਿਊਮਰ ਇਮਿਊਨ ਪ੍ਰਤੀਕ੍ਰਿਆਵਾਂ ਨੂੰ ਸ਼ਾਮਲ ਕਰਦਾ ਹੈ।ਡੈਲੀਟੈਕਟ ਪਹਿਲੀ ਤੀਜੀ ਪੀੜ੍ਹੀ ਦਾ ਔਨਕੋਲੀਟਿਕ HSV-1 ਹੈ ਜੋ ਵਰਤਮਾਨ ਵਿੱਚ ਕਲੀਨਿਕਲ ਮੁਲਾਂਕਣ ਵਿੱਚ ਹੈ।ਜਾਪਾਨ ਵਿੱਚ ਡੇਲੀਟੈਕਟ ਦੀ ਪ੍ਰਵਾਨਗੀ ਸਿੰਗਲ-ਆਰਮ ਫੇਜ਼ 2 ਕਲੀਨਿਕਲ ਅਜ਼ਮਾਇਸ਼ 'ਤੇ ਅਧਾਰਤ ਸੀ।ਆਵਰਤੀ ਗਲਾਈਓਬਲਾਸਟੋਮਾ ਵਾਲੇ ਮਰੀਜ਼ਾਂ ਵਿੱਚ, ਡੇਲੀਟੈਕਟ ਨੇ ਇੱਕ ਸਾਲ ਦੇ ਬਚਾਅ ਦੇ ਪ੍ਰਾਇਮਰੀ ਅੰਤਮ ਬਿੰਦੂ ਨੂੰ ਪੂਰਾ ਕੀਤਾ, ਅਤੇ ਨਤੀਜਿਆਂ ਨੇ ਦਿਖਾਇਆ ਕਿ ਡੇਲੀਟੈਕਟ ਨੇ G207 ਨਾਲੋਂ ਵਧੀਆ ਪ੍ਰਦਰਸ਼ਨ ਕੀਤਾ।ਮਜ਼ਬੂਤ ਪ੍ਰਤੀਕ੍ਰਿਤੀ ਅਤੇ ਉੱਚ ਐਂਟੀਟਿਊਮਰ ਗਤੀਵਿਧੀ.ਇਹ ਠੋਸ ਟਿਊਮਰ ਮਾਡਲਾਂ ਵਿੱਚ ਪ੍ਰਭਾਵੀ ਹੈ ਜਿਸ ਵਿੱਚ ਛਾਤੀ, ਪ੍ਰੋਸਟੇਟ, ਸਕਵਾਨੋਮਾ, ਨੈਸੋਫੈਰਨਜੀਅਲ, ਹੈਪੇਟੋਸੈਲੂਲਰ, ਕੋਲੋਰੈਕਟਲ, ਘਾਤਕ ਪੈਰੀਫਿਰਲ ਨਰਵ ਸੀਥ ਟਿਊਮਰ ਅਤੇ ਥਾਇਰਾਇਡ ਕੈਂਸਰ ਸ਼ਾਮਲ ਹਨ।
(9) ਉਪਸਟਾਜ਼ਾ
ਕੰਪਨੀ: PTC Therapeutics, Inc. (NASDAQ: PTCT) ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਜੁਲਾਈ 2022 ਵਿੱਚ ਈਯੂ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਸੁਗੰਧਿਤ ਐਲ-ਐਮੀਨੋ ਐਸਿਡ ਡੀਕਾਰਬੋਕਸੀਲੇਸ (ਏਏਡੀਸੀ) ਦੀ ਘਾਟ ਲਈ, 18 ਮਹੀਨਿਆਂ ਅਤੇ ਇਸ ਤੋਂ ਵੱਧ ਉਮਰ ਦੇ ਮਰੀਜ਼ਾਂ ਦੇ ਇਲਾਜ ਲਈ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ ਹੈ।
ਟਿੱਪਣੀਆਂ: Upstaza™ (eladocagene exuparvovec) ਇੱਕ ਵੈਕਟਰ ਦੇ ਤੌਰ 'ਤੇ ਐਡੀਨੋ-ਐਸੋਸੀਏਟਿਡ ਵਾਇਰਸ ਟਾਈਪ 2 (AAV2) ਦੀ ਵਰਤੋਂ ਕਰਦੇ ਹੋਏ ਵੀਵੋ ਜੀਨ ਥੈਰੇਪੀ ਹੈ।ਏਏਡੀਸੀ ਐਨਜ਼ਾਈਮ ਨੂੰ ਏਨਕੋਡਿੰਗ ਕਰਨ ਵਾਲੇ ਜੀਨ ਵਿੱਚ ਪਰਿਵਰਤਨ ਦੇ ਕਾਰਨ ਮਰੀਜ਼ ਬਿਮਾਰ ਹੈ।AAV2 AADC ਐਨਜ਼ਾਈਮ ਨੂੰ ਏਨਕੋਡਿੰਗ ਕਰਨ ਵਾਲਾ ਇੱਕ ਸਿਹਤਮੰਦ ਜੀਨ ਰੱਖਦਾ ਹੈ।ਉਪਚਾਰਕ ਪ੍ਰਭਾਵ ਜੈਨੇਟਿਕ ਮੁਆਵਜ਼ੇ ਦੇ ਰੂਪ ਵਿੱਚ ਪ੍ਰਾਪਤ ਕੀਤਾ ਜਾਂਦਾ ਹੈ.ਸਿਧਾਂਤ ਵਿੱਚ, ਇੱਕ ਸਿੰਗਲ ਖੁਰਾਕ ਲੰਬੇ ਸਮੇਂ ਲਈ ਪ੍ਰਭਾਵਸ਼ਾਲੀ ਹੁੰਦੀ ਹੈ।ਇਹ ਪਹਿਲੀ ਮਾਰਕੀਟਡ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜੋ ਦਿਮਾਗ ਵਿੱਚ ਸਿੱਧਾ ਟੀਕਾ ਲਗਾਇਆ ਜਾਂਦਾ ਹੈ।ਮਾਰਕੀਟਿੰਗ ਅਧਿਕਾਰ ਸਾਰੇ 27 EU ਮੈਂਬਰ ਰਾਜਾਂ ਦੇ ਨਾਲ-ਨਾਲ ਆਈਸਲੈਂਡ, ਨਾਰਵੇ ਅਤੇ ਲੀਚਨਸਟਾਈਨ 'ਤੇ ਲਾਗੂ ਹੁੰਦਾ ਹੈ।
(9) ਰੌਕਟੇਵੀਅਨ
ਕੰਪਨੀ: BioMarin ਫਾਰਮਾਸਿਊਟੀਕਲ (BioMarin) ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤਾ ਗਿਆ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਅਗਸਤ 2022 ਵਿੱਚ ਈਯੂ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਗੰਭੀਰ ਹੀਮੋਫਿਲੀਆ ਏ ਵਾਲੇ ਬਾਲਗ ਮਰੀਜ਼ਾਂ ਦੇ ਇਲਾਜ ਲਈ ਬਿਨਾਂ FVIII ਫੈਕਟਰ ਇਨਿਬਿਸ਼ਨ ਅਤੇ AAV5 ਐਂਟੀਬਾਡੀ ਨੈਗੇਟਿਵ ਦੇ ਇਤਿਹਾਸ ਦੇ ਬਿਨਾਂ।
ਟਿੱਪਣੀਆਂ: Roctavian (valoctocogene roxaparvovec) AAV5 ਨੂੰ ਵੈਕਟਰ ਦੇ ਤੌਰ 'ਤੇ ਵਰਤਦਾ ਹੈ ਅਤੇ ਬੀ ਡੋਮੇਨ ਨੂੰ ਮਿਟਾਉਣ ਦੇ ਨਾਲ ਮਨੁੱਖੀ ਕੋਗੂਲੇਸ਼ਨ ਫੈਕਟਰ ਅੱਠ (FVIII) ਦੇ ਸਮੀਕਰਨ ਨੂੰ ਚਲਾਉਣ ਲਈ ਮਨੁੱਖੀ ਜਿਗਰ-ਵਿਸ਼ੇਸ਼ ਪ੍ਰਮੋਟਰ HLP ਦੀ ਵਰਤੋਂ ਕਰਦਾ ਹੈ।ਵੈਲਕਟੋਕੋਜੀਨ ਰੋਕਸਾਪਰਵੋਵੇਕ ਦੀ ਮਾਰਕੀਟਿੰਗ ਨੂੰ ਮਨਜ਼ੂਰੀ ਦੇਣ ਲਈ ਯੂਰਪੀਅਨ ਕਮਿਸ਼ਨ ਦਾ ਫੈਸਲਾ ਡਰੱਗ ਦੇ ਕਲੀਨਿਕਲ ਵਿਕਾਸ ਪ੍ਰੋਗਰਾਮ ਦੇ ਸਮੁੱਚੇ ਡੇਟਾ 'ਤੇ ਅਧਾਰਤ ਹੈ।ਉਹਨਾਂ ਵਿੱਚੋਂ, ਪੜਾਅ III ਕਲੀਨਿਕਲ ਅਜ਼ਮਾਇਸ਼ GENEr8-1 ਨੇ ਦਿਖਾਇਆ ਕਿ ਨਾਮਾਂਕਣ ਤੋਂ ਪਹਿਲਾਂ ਦੇ ਸਾਲ ਦੇ ਅੰਕੜਿਆਂ ਦੀ ਤੁਲਨਾ ਵਿੱਚ, valoctocogene roxaparvovec ਦੇ ਇੱਕ ਨਿਵੇਸ਼ ਦੇ ਬਾਅਦ, ਵਿਸ਼ਿਆਂ ਵਿੱਚ ਇੱਕ ਮਹੱਤਵਪੂਰਨ ਤੌਰ 'ਤੇ ਘੱਟ ਸਾਲਾਨਾ ਖੂਨ ਵਹਿਣ ਦੀ ਦਰ (ABR), ਰੀਕੌਂਬੀਨੈਂਟ ਫੈਕਟਰ VIII (F8) ਦੀ ਘੱਟ ਵਾਰ-ਵਾਰ ਵਰਤੋਂ, ਖੂਨ ਦੀਆਂ ਤਿਆਰੀਆਂ ਵਿੱਚ ਇੱਕ ਮਹੱਤਵਪੂਰਣ ਪ੍ਰੋਟੀਨ ਸਰਗਰਮੀ ਨੂੰ ਵਧਾਉਂਦੀ ਹੈ, ਜਾਂ F8.ਇਲਾਜ ਦੇ 4 ਹਫ਼ਤਿਆਂ ਤੋਂ ਬਾਅਦ, ਵਿਸ਼ਿਆਂ ਦੀ ਸਾਲਾਨਾ F8 ਵਰਤੋਂ ਅਤੇ ਇਲਾਜ ਦੀ ਲੋੜ ਵਾਲੇ ABR ਨੂੰ ਕ੍ਰਮਵਾਰ 99% ਅਤੇ 84% ਘਟਾ ਦਿੱਤਾ ਗਿਆ, ਇੱਕ ਅੰਕੜਾਤਮਕ ਤੌਰ 'ਤੇ ਮਹੱਤਵਪੂਰਨ ਅੰਤਰ (p<0.001)।ਸੁਰੱਖਿਆ ਪ੍ਰੋਫਾਈਲ ਅਨੁਕੂਲ ਸੀ, ਜਿਸ ਵਿੱਚ ਕੋਈ ਵੀ ਵਿਸ਼ਿਆਂ ਨੂੰ F8 ਕਾਰਕ ਰੋਕ, ਖ਼ਤਰਨਾਕਤਾ, ਜਾਂ ਥ੍ਰੋਮੋਬੋਟਿਕ ਮਾੜੇ ਪ੍ਰਭਾਵਾਂ ਦਾ ਅਨੁਭਵ ਨਹੀਂ ਕੀਤਾ ਗਿਆ ਸੀ, ਅਤੇ ਕੋਈ ਇਲਾਜ ਸੰਬੰਧੀ ਗੰਭੀਰ ਪ੍ਰਤੀਕੂਲ ਘਟਨਾਵਾਂ (SAEs) ਦੀ ਰਿਪੋਰਟ ਨਹੀਂ ਕੀਤੀ ਗਈ ਸੀ।
3. ਛੋਟੀਆਂ ਨਿਊਕਲੀਕ ਐਸਿਡ ਦਵਾਈਆਂ
(1) ਵੀਤਰਾਵੇਨ
ਕੰਪਨੀ: ਆਇਓਨਿਸ ਫਾਰਮਾ (ਪਹਿਲਾਂ ਆਈਸਿਸ ਫਾਰਮਾ) ਅਤੇ ਨੋਵਾਰਟਿਸ ਦੁਆਰਾ ਸਾਂਝੇ ਤੌਰ 'ਤੇ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਹੈ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: 1998 ਅਤੇ 1999 ਵਿੱਚ FDA ਅਤੇ EU EMA ਦੁਆਰਾ ਪ੍ਰਵਾਨਿਤ।
ਸੰਕੇਤ: ਐੱਚਆਈਵੀ-ਸਕਾਰਾਤਮਕ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਸਾਇਟੋਮੇਗਲੋਵਾਇਰਸ ਰੀਟੀਨਾਈਟਿਸ ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਵਿਟਰਾਵੇਨ ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਦਵਾਈ ਹੈ ਅਤੇ ਦੁਨੀਆ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਪ੍ਰਵਾਨਿਤ ਪਹਿਲੀ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਦਵਾਈ ਹੈ।ਮਾਰਕੀਟ ਦੀ ਸ਼ੁਰੂਆਤ ਵਿੱਚ, ਐਂਟੀ-ਸਾਈਟੋਮੇਗਲੋਵਾਇਰਸ ਦਵਾਈਆਂ ਦੀ ਮਾਰਕੀਟ ਦੀ ਮੰਗ ਬਹੁਤ ਜ਼ਰੂਰੀ ਸੀ;ਫਿਰ ਬਹੁਤ ਜ਼ਿਆਦਾ ਸਰਗਰਮ ਐਂਟੀਰੇਟਰੋਵਾਇਰਲ ਥੈਰੇਪੀ ਦੇ ਵਿਕਾਸ ਦੇ ਕਾਰਨ, ਸਾਈਟੋਮੇਗਲੋਵਾਇਰਸ ਦੇ ਕੇਸਾਂ ਦੀ ਗਿਣਤੀ ਤੇਜ਼ੀ ਨਾਲ ਘਟ ਗਈ।ਮਾਰਕੀਟ ਦੀ ਘੱਟ ਮੰਗ ਦੇ ਕਾਰਨ, ਦਵਾਈ ਨੂੰ 2002 ਅਤੇ 2006 ਵਿੱਚ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੇ ਦੇਸ਼ਾਂ ਅਤੇ ਅਮਰੀਕਾ ਵਿੱਚ ਵਾਪਸ ਲੈਣ ਲਈ ਜਾਰੀ ਕੀਤਾ ਗਿਆ ਸੀ।
(2) ਮੈਕੁਜੇਨ
ਕੰਪਨੀ: Pfizer ਅਤੇ Eyetech ਦੁਆਰਾ ਸਹਿ-ਵਿਕਸਤ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2004 ਵਿੱਚ ਸੰਯੁਕਤ ਰਾਜ ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਨਿਓਵੈਸਕੁਲਰ ਉਮਰ-ਸਬੰਧਤ ਮੈਕੁਲਰ ਡੀਜਨਰੇਸ਼ਨ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਮੈਕਯੂਜੇਨ ਇੱਕ ਪੈਗਾਈਲੇਟਿਡ ਸੰਸ਼ੋਧਿਤ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ ਜੋ ਵੈਸਕੁਲਰ ਐਂਡੋਥੈਲੀਅਲ ਗਰੋਥ ਫੈਕਟਰ (VEGF165 isoform) ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾ ਸਕਦੀ ਹੈ ਅਤੇ ਜੋੜ ਸਕਦੀ ਹੈ, ਅਤੇ ਇਸਨੂੰ ਇੰਟਰਾਵਿਟ੍ਰੀਅਲ ਇੰਜੈਕਸ਼ਨ ਦੁਆਰਾ ਚਲਾਇਆ ਜਾਂਦਾ ਹੈ।
(3) ਡਿਫਿਟੇਲੀਓ
ਕੰਪਨੀ: ਜੈਜ਼ ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: 2013 ਵਿੱਚ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੁਆਰਾ ਪ੍ਰਵਾਨਿਤ, ਅਤੇ ਮਾਰਚ 2016 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਹੇਮੇਟੋਪੋਏਟਿਕ ਸਟੈਮ ਸੈੱਲ ਟ੍ਰਾਂਸਪਲਾਂਟੇਸ਼ਨ ਤੋਂ ਬਾਅਦ ਗੁਰਦੇ ਜਾਂ ਪਲਮਨਰੀ ਨਪੁੰਸਕਤਾ ਨਾਲ ਸੰਬੰਧਿਤ ਹੈਪੇਟਿਕ ਵੇਨਿਊਲ ਓਕਲੂਸਿਵ ਬਿਮਾਰੀ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਡਿਫਿਟੇਲੀਓ ਇੱਕ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ, ਪਲਾਜ਼ਮਿਨ ਵਿਸ਼ੇਸ਼ਤਾਵਾਂ ਵਾਲੇ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡਸ ਦਾ ਮਿਸ਼ਰਣ।ਇਸ ਨੂੰ ਵਪਾਰਕ ਕਾਰਨਾਂ ਕਰਕੇ 2009 ਵਿੱਚ ਵਾਪਸ ਲੈ ਲਿਆ ਗਿਆ ਸੀ।
(4) ਕਿਨਮਰੋ
ਕੰਪਨੀ: ਆਇਓਨਿਸ ਫਾਰਮਾ ਅਤੇ ਕੈਸਟਲ ਦੁਆਰਾ ਸਹਿ-ਵਿਕਸਤ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: ਸੰਯੁਕਤ ਰਾਜ ਵਿੱਚ 2013 ਵਿੱਚ ਇੱਕ ਅਨਾਥ ਦਵਾਈ ਦੇ ਰੂਪ ਵਿੱਚ ਪ੍ਰਵਾਨਿਤ।
ਸੰਕੇਤ: ਹੋਮੋਜ਼ਾਈਗਸ ਫੈਮਿਲੀਅਲ ਹਾਈਪਰਕੋਲੇਸਟ੍ਰੋਲੇਮੀਆ ਦੇ ਸਹਾਇਕ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਕਾਇਨਮਰੋ ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ, ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਮਨੁੱਖੀ apo B-100 mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦਾ ਹੈ।ਕੀਨਮਰੋ ਨੂੰ ਹਫ਼ਤੇ ਵਿੱਚ ਇੱਕ ਵਾਰ 200 ਮਿਲੀਗ੍ਰਾਮ ਦੇ ਰੂਪ ਵਿੱਚ ਸਬਕੁਟੇਨਿਊਸ ਦੇ ਰੂਪ ਵਿੱਚ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ।
(5) ਸਪਿਨਰਾਜ਼ਾ
ਕੰਪਨੀ: Ionis Pharmaceuticals ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: ਦਸੰਬਰ 2016 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਰੀੜ੍ਹ ਦੀ ਮਾਸਪੇਸ਼ੀ ਐਟ੍ਰੋਫੀ (SMA) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਸਪਿਨਰਾਜ਼ਾ (ਨੁਸਿਨਰਸੇਨ) ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ।ਸਪਿਨਰਾਜ਼ਾ ਐਸਐਮਐਨ2 ਜੀਨ ਦੇ ਆਰਐਨਏ ਸਪਲਿਸਿੰਗ ਨੂੰ ਐਸਐਮਐਨ2 ਐਕਸੋਨ 7 ਦੀ ਸਪਲਿਸਿੰਗ ਸਾਈਟ ਨਾਲ ਬੰਨ੍ਹ ਕੇ ਬਦਲ ਸਕਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਪੂਰੀ ਤਰ੍ਹਾਂ ਕਾਰਜਸ਼ੀਲ SMN ਪ੍ਰੋਟੀਨ ਦਾ ਉਤਪਾਦਨ ਵਧਦਾ ਹੈ।ਅਗਸਤ 2016 ਵਿੱਚ, BIOGEN ਕਾਰਪੋਰੇਸ਼ਨ ਨੇ ਸਪਿਨਰਾਜ਼ਾ ਦੇ ਗਲੋਬਲ ਅਧਿਕਾਰਾਂ ਨੂੰ ਪ੍ਰਾਪਤ ਕਰਨ ਲਈ ਆਪਣੇ ਵਿਕਲਪ ਦੀ ਵਰਤੋਂ ਕੀਤੀ।ਸਪਿਨਰਾਜ਼ਾ ਨੇ 2011 ਵਿੱਚ ਮਨੁੱਖਾਂ ਵਿੱਚ ਆਪਣਾ ਪਹਿਲਾ ਕਲੀਨਿਕਲ ਅਜ਼ਮਾਇਸ਼ ਸ਼ੁਰੂ ਕੀਤਾ ਸੀ। ਸਿਰਫ਼ 5 ਸਾਲਾਂ ਵਿੱਚ, ਇਸਨੂੰ 2016 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ ਸੀ, ਜੋ FDA ਦੁਆਰਾ ਇਸਦੀ ਪ੍ਰਭਾਵਸ਼ੀਲਤਾ ਦੀ ਪੂਰੀ ਮਾਨਤਾ ਨੂੰ ਦਰਸਾਉਂਦਾ ਹੈ।ਦਵਾਈ ਨੂੰ ਅਪ੍ਰੈਲ 2019 ਵਿੱਚ ਚੀਨ ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ ਸੀ। ਚੀਨ ਵਿੱਚ ਸਪਿਨਰਾਜ਼ਾ ਦਾ ਪੂਰਾ ਮਨਜ਼ੂਰੀ ਚੱਕਰ 6 ਮਹੀਨਿਆਂ ਤੋਂ ਘੱਟ ਹੈ।ਸਪਿਨਰਾਜ਼ਾ ਨੂੰ ਸੰਯੁਕਤ ਰਾਜ ਵਿੱਚ ਪਹਿਲੀ ਵਾਰ ਮਨਜ਼ੂਰ ਹੋਏ 2 ਸਾਲ ਅਤੇ 2 ਮਹੀਨੇ ਹੋ ਗਏ ਹਨ।ਅਜਿਹੀ ਬਲਾਕਬਸਟਰ ਵਿਦੇਸ਼ੀ ਦੁਰਲੱਭ ਬਿਮਾਰੀ ਦੀ ਨਵੀਂ ਦਵਾਈ ਚੀਨ ਵਿੱਚ ਸੂਚੀਬੱਧ ਹੋਣ ਦੀ ਗਤੀ ਪਹਿਲਾਂ ਹੀ ਬਹੁਤ ਤੇਜ਼ ਹੈ।ਇਹ 1 ਨਵੰਬਰ, 2018 ਨੂੰ ਸੈਂਟਰ ਫਾਰ ਡਰੱਗ ਇਵੈਲੂਏਸ਼ਨ ਦੁਆਰਾ ਜਾਰੀ ਕੀਤੇ ਗਏ "ਓਵਰਸੀਜ਼ ਨਵੀਆਂ ਦਵਾਈਆਂ ਦੀ ਪਹਿਲੀ ਸੂਚੀ ਦੇ ਜਾਰੀ ਹੋਣ 'ਤੇ ਨੋਟਿਸ' ਦੇ ਕਾਰਨ ਵੀ ਹੈ, ਜੋ ਕਿ 1 ਨਵੰਬਰ, 2018 ਨੂੰ ਜਾਰੀ ਕੀਤੀ ਗਈ ਸੀ, ਜਿਸ ਨੂੰ ਤੇਜ਼ ਸਮੀਖਿਆ ਲਈ 40 ਮੁੱਖ ਵਿਦੇਸ਼ੀ ਨਵੀਆਂ ਦਵਾਈਆਂ ਦੇ ਪਹਿਲੇ ਬੈਚ ਵਿੱਚ ਸ਼ਾਮਲ ਕੀਤਾ ਗਿਆ ਸੀ, ਅਤੇ ਸਪਿਨਰਾਜ਼ਾ ਨੂੰ ਰੈਂਕ ਦਿੱਤਾ ਗਿਆ ਸੀ।
(6) ਐਕਸੈਂਡਿਸ 51
ਕੰਪਨੀ: AVI BioPharma (ਬਾਅਦ ਵਿੱਚ Sarepta Therapeutics ਨਾਮ ਦਿੱਤਾ ਗਿਆ) ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: ਸਤੰਬਰ 2016 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਐਕਸੋਨ 51 ਸਕਿਪਿੰਗ ਜੀਨ ਵਿੱਚ ਡੀਐਮਡੀ ਜੀਨ ਪਰਿਵਰਤਨ ਦੇ ਨਾਲ ਡੁਕੇਨ ਮਾਸਕੂਲਰ ਡਾਈਸਟ੍ਰੋਫੀ (ਡੀਐਮਡੀ) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: Exondys 51 ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ।ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡੀਐਮਡੀ ਜੀਨ ਦੇ ਪੂਰਵ-mRNA ਦੀ ਐਕਸੋਨ 51 ਸਥਿਤੀ ਨਾਲ ਬੰਨ੍ਹ ਸਕਦਾ ਹੈ, ਨਤੀਜੇ ਵਜੋਂ ਪਰਿਪੱਕ mRNA ਬਣਦਾ ਹੈ।ਐਕਸਾਈਜ਼ਨ, ਇਸ ਤਰ੍ਹਾਂ mRNA ਰੀਡਿੰਗ ਫ੍ਰੇਮ ਨੂੰ ਅੰਸ਼ਕ ਤੌਰ 'ਤੇ ਠੀਕ ਕਰਦਾ ਹੈ, ਮਰੀਜ਼ ਨੂੰ ਡਾਇਸਟ੍ਰੋਫਿਨ ਦੇ ਕੁਝ ਕਾਰਜਸ਼ੀਲ ਰੂਪਾਂ ਦਾ ਸੰਸਲੇਸ਼ਣ ਕਰਨ ਵਿੱਚ ਮਦਦ ਕਰਦਾ ਹੈ ਜੋ ਆਮ ਪ੍ਰੋਟੀਨ ਨਾਲੋਂ ਛੋਟੇ ਹੁੰਦੇ ਹਨ, ਜਿਸ ਨਾਲ ਮਰੀਜ਼ ਦੇ ਲੱਛਣਾਂ ਵਿੱਚ ਸੁਧਾਰ ਹੁੰਦਾ ਹੈ।
(7) ਤੇਗਸੇਦੀ
ਕੰਪਨੀ: Ionis Pharmaceuticals ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਜੁਲਾਈ 2018 ਵਿੱਚ ਮਾਰਕੀਟਿੰਗ ਲਈ ਯੂਰਪੀਅਨ ਯੂਨੀਅਨ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਖ਼ਾਨਦਾਨੀ transthyretin amyloidosis (hATTR) ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਟੈਗਸੇਡੀ ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ ਜੋ ਟ੍ਰਾਂਸਥਾਈਰੇਟਿਨ mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ।ਇਹ HATTR ਦੇ ਇਲਾਜ ਲਈ ਦੁਨੀਆ ਦੀ ਪਹਿਲੀ ਪ੍ਰਵਾਨਿਤ ਦਵਾਈ ਹੈ।ਪ੍ਰਸ਼ਾਸਨ ਦੀ ਵਿਧੀ ਚਮੜੀ ਦੇ ਹੇਠਲੇ ਟੀਕੇ ਹੈ.ਡਰੱਗ ਟ੍ਰਾਂਸਥਾਈਰੇਟਿਨ (ATTR) ਦੇ mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾ ਕੇ ATTR ਪ੍ਰੋਟੀਨ ਦੇ ਉਤਪਾਦਨ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ, ਅਤੇ ATTR ਦੇ ਇਲਾਜ ਵਿੱਚ ਇੱਕ ਚੰਗਾ ਲਾਭ-ਜੋਖਮ ਅਨੁਪਾਤ ਹੈ।ਨਾ ਤਾਂ ਬਿਮਾਰੀ ਦਾ ਪੜਾਅ ਅਤੇ ਨਾ ਹੀ ਕਾਰਡੀਓਮਿਓਪੈਥੀ ਦੀ ਮੌਜੂਦਗੀ ਸੰਬੰਧਿਤ ਸੀ।
(8) ਓਨਪੈਟਰੋ
ਕੰਪਨੀ: ਅਲਨੈਲਮ ਅਤੇ ਸਨੋਫੀ ਦੁਆਰਾ ਸਹਿ-ਵਿਕਸਤ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: 2018 ਵਿੱਚ ਸੰਯੁਕਤ ਰਾਜ ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਖ਼ਾਨਦਾਨੀ transthyretin amyloidosis (hATTR) ਦੇ ਇਲਾਜ ਲਈ.
ਟਿੱਪਣੀਆਂ: ਓਨਪੈਟ੍ਰੋ ਇੱਕ siRNA ਡਰੱਗ ਹੈ ਜੋ ਟ੍ਰਾਂਸਥਾਈਰੇਟਿਨ mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ, ਜੋ ਕਿ ਜਿਗਰ ਵਿੱਚ ATTR ਪ੍ਰੋਟੀਨ ਦੇ ਉਤਪਾਦਨ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ ਅਤੇ transthyretin (ATTR) ਦੇ mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾ ਕੇ ਪੈਰੀਫਿਰਲ ਨਸਾਂ ਵਿੱਚ ਐਮੀਲੋਇਡ ਜਮ੍ਹਾਂ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ।, ਇਸ ਤਰ੍ਹਾਂ ਬਿਮਾਰੀ ਦੇ ਲੱਛਣਾਂ ਵਿੱਚ ਸੁਧਾਰ ਅਤੇ ਰਾਹਤ.
(9) ਗਿਵਲਾਰੀ
ਕੰਪਨੀ: ਅਲਨੈਲਮ ਕਾਰਪੋਰੇਸ਼ਨ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਹੈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਨਵੰਬਰ 2019 ਵਿੱਚ ਐਫ ਡੀ ਏ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਬਾਲਗਾਂ ਵਿੱਚ ਤੀਬਰ ਹੈਪੇਟਿਕ ਪੋਰਫਾਈਰੀਆ (ਏਐਚਪੀ) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਗਿਵਲਾਰੀ ਇੱਕ siRNA ਦਵਾਈ ਹੈ, ਓਨਪੈਟ੍ਰੋ ਤੋਂ ਬਾਅਦ ਮਾਰਕੀਟਿੰਗ ਲਈ ਪ੍ਰਵਾਨਿਤ ਦੂਜੀ siRNA ਦਵਾਈ ਹੈ।ਡਰੱਗ ਨੂੰ ਚਮੜੀ ਦੇ ਹੇਠਾਂ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ ਅਤੇ ALAS1 ਪ੍ਰੋਟੀਨ ਦੇ ਨਿਘਾਰ ਲਈ mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦਾ ਹੈ।ਮਾਸਿਕ ਗਿਵਲਾਰੀ ਇਲਾਜ ਜਿਗਰ ਵਿੱਚ ALAS1 ਦੇ ਪੱਧਰ ਨੂੰ ਮਹੱਤਵਪੂਰਨ ਅਤੇ ਲਗਾਤਾਰ ਘਟਾ ਸਕਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਨਿਊਰੋਟੌਕਸਿਕ ALA ਅਤੇ PBG ਦੇ ਪੱਧਰਾਂ ਨੂੰ ਆਮ ਸੀਮਾ ਤੱਕ ਘਟਾਇਆ ਜਾ ਸਕਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਮਰੀਜ਼ ਦੀ ਬਿਮਾਰੀ ਦੇ ਲੱਛਣਾਂ ਤੋਂ ਰਾਹਤ ਮਿਲਦੀ ਹੈ।ਅੰਕੜੇ ਦਰਸਾਉਂਦੇ ਹਨ ਕਿ ਗਿਵਲਾਰੀ ਨਾਲ ਇਲਾਜ ਕੀਤੇ ਗਏ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਪਲੇਸਬੋ ਸਮੂਹ ਦੇ ਮੁਕਾਬਲੇ ਬਿਮਾਰੀ ਦੇ ਭੜਕਣ ਦੀ ਗਿਣਤੀ ਵਿੱਚ 74% ਦੀ ਕਮੀ ਆਈ ਹੈ।
(10) ਵਯੋਂਡਿਸ53
ਕੰਪਨੀ: ਸਰੇਪਟਾ ਥੈਰੇਪਿਊਟਿਕਸ ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: ਦਸੰਬਰ 2019 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਡਾਇਸਟ੍ਰੋਫਿਨ ਜੀਨ ਐਕਸੋਨ 53 ਸਪਲਾਇਸ ਮਿਊਟੇਸ਼ਨ ਵਾਲੇ ਡੀਐਮਡੀ ਮਰੀਜ਼ਾਂ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਵਯੋਂਡਿਸ 53 ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ।ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਡਾਇਸਟ੍ਰੋਫਿਨ mRNA ਪੂਰਵਗਾਮੀ ਦੀ ਸਪਲੀਸਿੰਗ ਪ੍ਰਕਿਰਿਆ ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ।ਡਾਇਸਟ੍ਰੋਫਿਨ mRNA ਪੂਰਵਗਾਮੀ ਦੀ ਅਸਿੱਧੇ ਪ੍ਰਕਿਰਿਆ ਵਿੱਚ, ਬਾਹਰੀ Exon 53 ਨੂੰ ਅੰਸ਼ਕ ਤੌਰ 'ਤੇ ਵੰਡਿਆ ਗਿਆ ਸੀ, ਭਾਵ ਪਰਿਪੱਕ mRNA 'ਤੇ ਮੌਜੂਦ ਨਹੀਂ, ਅਤੇ ਇੱਕ ਕੱਟਿਆ ਹੋਇਆ ਪਰ ਅਜੇ ਵੀ ਕਾਰਜਸ਼ੀਲ ਡਾਇਸਟ੍ਰੋਫਿਨ ਪ੍ਰੋਟੀਨ ਪੈਦਾ ਕਰਨ ਲਈ ਤਿਆਰ ਕੀਤਾ ਗਿਆ ਸੀ, ਜਿਸ ਨਾਲ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਕਸਰਤ ਦੀ ਸਮਰੱਥਾ ਵਿੱਚ ਸੁਧਾਰ ਹੁੰਦਾ ਹੈ।
(11) ਵੇਲੀਵਰਾ
ਕੰਪਨੀ: Ionis Pharmaceuticals ਅਤੇ ਇਸਦੀ ਸਹਾਇਕ ਕੰਪਨੀ Akcea Therapeutics ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਮਈ 2019 ਵਿੱਚ ਯੂਰਪੀਅਨ ਮੈਡੀਸਨ ਏਜੰਸੀ (EMA) ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਪਰਿਵਾਰਕ chylomicronemia ਸਿੰਡਰੋਮ (FCS) ਵਾਲੇ ਬਾਲਗ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਇੱਕ ਨਿਯੰਤਰਿਤ ਖੁਰਾਕ ਲਈ ਇੱਕ ਸਹਾਇਕ ਥੈਰੇਪੀ ਵਜੋਂ।
ਟਿੱਪਣੀਆਂ: ਵੇਲੀਵਰਾ ਇੱਕ ਐਂਟੀਸੈਂਸ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ, ਜੋ ਕਿ ਦੁਨੀਆ ਵਿੱਚ FCS ਦੇ ਇਲਾਜ ਲਈ ਪ੍ਰਵਾਨਿਤ ਪਹਿਲੀ ਦਵਾਈ ਹੈ।
(12) ਲੇਕਵੀਓ
ਕੰਪਨੀ: ਨੋਵਾਰਟਿਸ ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਦਸੰਬਰ 2020 ਵਿੱਚ ਈਯੂ ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਬਾਲਗ ਪ੍ਰਾਇਮਰੀ ਹਾਈਪਰਕੋਲੇਸਟ੍ਰੋਲੇਮੀਆ (ਹੀਟਰੋਜ਼ਾਈਗਸ ਪਰਿਵਾਰਕ ਅਤੇ ਗੈਰ-ਪਰਿਵਾਰਕ) ਜਾਂ ਮਿਸ਼ਰਤ ਡਿਸਲਿਪੀਡਮੀਆ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਲੇਕਵੀਓ ਇੱਕ siRNA ਡਰੱਗ ਹੈ ਜੋ PCSK9 mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ।ਇਹ ਦੁਨੀਆ ਦੀ ਪਹਿਲੀ ਕੋਲੈਸਟ੍ਰੋਲ-ਘੱਟ ਕਰਨ ਵਾਲੀ (LDL-C) siRNA ਥੈਰੇਪੀ ਹੈ।ਪ੍ਰਸ਼ਾਸਨ ਦੀ ਵਿਧੀ ਚਮੜੀ ਦੇ ਹੇਠਲੇ ਟੀਕੇ ਹੈ.ਦਵਾਈ PCSK9 ਪ੍ਰੋਟੀਨ ਦੇ ਪੱਧਰਾਂ ਨੂੰ ਘਟਾਉਣ ਲਈ RNA ਦਖਲਅੰਦਾਜ਼ੀ ਦੁਆਰਾ ਕੰਮ ਕਰਦੀ ਹੈ, ਜੋ ਬਦਲੇ ਵਿੱਚ LDL-C ਪੱਧਰਾਂ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ।ਕਲੀਨਿਕਲ ਡੇਟਾ ਦਰਸਾਉਂਦੇ ਹਨ ਕਿ ਲੇਕਵੀਓ ਉਹਨਾਂ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਲਗਭਗ 50% ਤੱਕ LDL-C ਨੂੰ ਘਟਾ ਸਕਦਾ ਹੈ ਜਿਨ੍ਹਾਂ ਦੇ LDL-C ਪੱਧਰਾਂ ਨੂੰ ਸਟੈਟਿਨਸ ਦੀ ਵੱਧ ਤੋਂ ਵੱਧ ਸਹਿਣਸ਼ੀਲ ਖੁਰਾਕਾਂ ਦੇ ਬਾਵਜੂਦ ਟੀਚੇ ਦੇ ਪੱਧਰ ਤੱਕ ਨਹੀਂ ਘਟਾਇਆ ਜਾ ਸਕਦਾ ਹੈ।
(13) ਔਕਸਲੂਮੋ
ਕੰਪਨੀ: ਅਲਨੈਲਮ ਫਾਰਮਾਸਿਊਟੀਕਲਜ਼ ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਨਵੰਬਰ 2020 ਵਿੱਚ EU ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਪ੍ਰਾਇਮਰੀ ਹਾਈਪਰੌਕਸਲੂਰੀਆ ਟਾਈਪ 1 (PH1) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਆਕਸਲੂਮੋ ਹਾਈਡ੍ਰੋਕਸੀ ਐਸਿਡ ਆਕਸੀਡੇਸ 1 (HAO1) mRNA ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਣ ਵਾਲੀ ਇੱਕ siRNA ਦਵਾਈ ਹੈ, ਜੋ ਕਿ ਚਮੜੀ ਦੇ ਹੇਠਾਂ ਦਿੱਤੀ ਜਾਂਦੀ ਹੈ।ਦਵਾਈ ਨੂੰ ਅਲਨੈਲਮ ਦੀ ਨਵੀਨਤਮ ਵਿਸਤ੍ਰਿਤ ਸਥਿਰਤਾ ਰਸਾਇਣਕ ESC-GalNAc ਸੰਜੋਗ ਤਕਨਾਲੋਜੀ ਦੀ ਵਰਤੋਂ ਕਰਕੇ ਵਿਕਸਤ ਕੀਤਾ ਗਿਆ ਸੀ, ਜੋ ਕਿ ਵਧੇਰੇ ਨਿਰੰਤਰਤਾ ਅਤੇ ਪ੍ਰਭਾਵਸ਼ੀਲਤਾ ਦੇ ਨਾਲ ਉਪ-ਚਲਣ ਦੁਆਰਾ ਸੰਚਾਲਿਤ siRNAs ਨੂੰ ਸਮਰੱਥ ਬਣਾਉਂਦਾ ਹੈ।ਇਹ ਦਵਾਈ ਹਾਈਡ੍ਰੋਕਸੀ ਐਸਿਡ ਆਕਸੀਡੇਸ 1 (HAO1) mRNA ਦੇ ਨਿਘਾਰ ਜਾਂ ਰੋਕ ਨੂੰ ਨਿਸ਼ਾਨਾ ਬਣਾਉਂਦੀ ਹੈ, ਜਿਗਰ ਵਿੱਚ ਗਲਾਈਕੋਲੇਟ ਆਕਸੀਡੇਸ ਦੇ ਪੱਧਰ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ, ਅਤੇ ਫਿਰ ਆਕਸਾਲੇਟ ਦੇ ਉਤਪਾਦਨ ਲਈ ਲੋੜੀਂਦੇ ਸਬਸਟਰੇਟ ਦੀ ਖਪਤ ਕਰਦੀ ਹੈ ਅਤੇ ਰੋਗ ਦੀ ਪ੍ਰਗਤੀ ਨੂੰ ਨਿਯੰਤਰਿਤ ਕਰਨ ਅਤੇ ਰੋਗੀਆਂ ਵਿੱਚ ਬਿਮਾਰੀ ਦੇ ਲੱਛਣਾਂ ਵਿੱਚ ਸੁਧਾਰ ਕਰਨ ਲਈ ਆਕਸਲੇਟ ਦੇ ਉਤਪਾਦਨ ਨੂੰ ਘਟਾਉਂਦੀ ਹੈ।
(14) Viltepso
ਕੰਪਨੀ: NS ਫਾਰਮਾ ਦੁਆਰਾ ਵਿਕਸਤ, ਨਿਪੋਨ ਸ਼ਿਨਯਾਕੂ ਦੀ ਸਹਾਇਕ ਕੰਪਨੀ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਅਗਸਤ 2020 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਐਕਸੋਨ 53 ਸਕਿੱਪਿੰਗ ਜੀਨ ਵਿੱਚ ਡੀਐਮਡੀ ਜੀਨ ਪਰਿਵਰਤਨ ਦੇ ਨਾਲ ਡੁਕੇਨ ਮਾਸਕੂਲਰ ਡਾਈਸਟ੍ਰੋਫੀ (ਡੀਐਮਡੀ) ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਵਿਲਟੇਪਸੋ ਇੱਕ ਫਾਸਫੋਰੋਡਿਆਮਾਈਡ ਮੋਰਫੋਲੀਨੋ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਹੈ।ਇਹ ਓਲੀਗੋਨਿਊਕਲੀਓਟਾਈਡ ਡਰੱਗ ਡੀਐਮਡੀ ਜੀਨ ਦੇ ਪ੍ਰੀ-mRNA ਦੀ ਐਕਸੋਨ 53 ਸਥਿਤੀ ਨਾਲ ਬੰਨ੍ਹ ਸਕਦੀ ਹੈ, ਨਤੀਜੇ ਵਜੋਂ ਪਰਿਪੱਕ mRNA ਬਣ ਸਕਦਾ ਹੈ।ਐਕਸੋਨ ਨੂੰ ਅੰਸ਼ਕ ਤੌਰ 'ਤੇ ਹਟਾ ਦਿੱਤਾ ਜਾਂਦਾ ਹੈ, ਜਿਸ ਨਾਲ ਐਮਆਰਐਨਏ ਰੀਡਿੰਗ ਫ੍ਰੇਮ ਨੂੰ ਅੰਸ਼ਕ ਤੌਰ 'ਤੇ ਠੀਕ ਕੀਤਾ ਜਾਂਦਾ ਹੈ, ਮਰੀਜ਼ ਨੂੰ ਡਾਇਸਟ੍ਰੋਫਿਨ ਦੇ ਕੁਝ ਕਾਰਜਸ਼ੀਲ ਰੂਪਾਂ ਨੂੰ ਸੰਸਲੇਸ਼ਣ ਕਰਨ ਵਿੱਚ ਮਦਦ ਕਰਦਾ ਹੈ ਜੋ ਆਮ ਪ੍ਰੋਟੀਨ ਨਾਲੋਂ ਛੋਟੇ ਹੁੰਦੇ ਹਨ, ਜਿਸ ਨਾਲ ਮਰੀਜ਼ ਦੇ ਲੱਛਣਾਂ ਵਿੱਚ ਸੁਧਾਰ ਹੁੰਦਾ ਹੈ।
(15) ਅਮਵੁਤਰਾ (ਵੁਟ੍ਰਿਸਿਰਨ)
ਕੰਪਨੀ: ਅਲਨੈਲਮ ਫਾਰਮਾਸਿਊਟੀਕਲਜ਼ ਦੁਆਰਾ ਵਿਕਸਿਤ ਕੀਤੀ ਗਈ।
ਮਾਰਕੀਟ ਕਰਨ ਦਾ ਸਮਾਂ: ਜੂਨ 2022 ਵਿੱਚ FDA ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਪੌਲੀਨਿਊਰੋਪੈਥੀ (hATTR-PN) ਦੇ ਨਾਲ ਬਾਲਗ ਖ਼ਾਨਦਾਨੀ ਟ੍ਰਾਂਸਥਾਈਰੇਟਿਨ ਐਮੀਲੋਇਡੋਸਿਸ ਦੇ ਇਲਾਜ ਲਈ।
ਟਿੱਪਣੀਆਂ: ਅਮਵੁਤਰਾ (ਵੁਟ੍ਰੀਸੀਰਨ) ਇੱਕ siRNA ਡਰੱਗ ਟਾਰਗੇਟਿੰਗ ਟ੍ਰਾਂਸਥਾਈਰੇਟਿਨ (ATTR) mRNA ਹੈ, ਜੋ ਕਿ ਸਬਕੁਟੇਨੀਅਸ ਇੰਜੈਕਸ਼ਨ ਦੁਆਰਾ ਚਲਾਈ ਜਾਂਦੀ ਹੈ।ਵੁਟ੍ਰੀਸੀਰਨ ਨੂੰ ਐਲਨੈਲਮ ਦੇ ਐਨਹਾਂਸਡ ਸਟੇਬਲਾਈਜ਼ੇਸ਼ਨ ਕੈਮਿਸਟਰੀ (ESC)-GalNAc ਕੰਜੁਗੇਟਿਡ ਡਿਲੀਵਰੀ ਪਲੇਟਫਾਰਮ ਦੇ ਆਧਾਰ 'ਤੇ ਵਧੀ ਹੋਈ ਤਾਕਤ ਅਤੇ ਮੈਟਾਬੋਲਿਕ ਸਥਿਰਤਾ ਦੇ ਨਾਲ ਤਿਆਰ ਕੀਤਾ ਗਿਆ ਹੈ।ਥੈਰੇਪੀ ਦੀ ਪ੍ਰਵਾਨਗੀ ਇਸਦੇ ਪੜਾਅ III ਕਲੀਨਿਕਲ ਅਧਿਐਨ (HELIOS-A) ਦੇ 9-ਮਹੀਨਿਆਂ ਦੇ ਅੰਕੜਿਆਂ 'ਤੇ ਅਧਾਰਤ ਹੈ, ਸਮੁੱਚੇ ਨਤੀਜੇ ਦਿਖਾਉਂਦੇ ਹਨ ਕਿ ਥੈਰੇਪੀ ਨੇ HATTR-PN ਦੇ ਲੱਛਣਾਂ ਵਿੱਚ ਸੁਧਾਰ ਕੀਤਾ ਹੈ, 50% ਤੋਂ ਵੱਧ ਮਰੀਜ਼ਾਂ ਦੇ ਉਲਟ ਜਾਂ ਪ੍ਰਗਤੀ ਨੂੰ ਰੋਕਣ ਦੇ ਨਾਲ।
4. ਹੋਰ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈਆਂ
(1) ਰੇਕਸਿਨ-ਜੀ
ਕੰਪਨੀ: Epeius Biotech ਦੁਆਰਾ ਵਿਕਸਤ.
ਮਾਰਕੀਟ ਲਈ ਸਮਾਂ: 2005 ਵਿੱਚ ਫਿਲੀਪੀਨ ਫੂਡ ਐਂਡ ਡਰੱਗ ਐਡਮਨਿਸਟ੍ਰੇਸ਼ਨ (BFAD) ਦੁਆਰਾ ਮਨਜ਼ੂਰ ਕੀਤਾ ਗਿਆ।
ਸੰਕੇਤ: ਉੱਨਤ ਕੈਂਸਰਾਂ ਦੇ ਇਲਾਜ ਲਈ ਜੋ ਕੀਮੋਥੈਰੇਪੀ ਪ੍ਰਤੀ ਰੋਧਕ ਹਨ।
ਟਿੱਪਣੀਆਂ: ਰੇਕਸਿਨ-ਜੀ ਇੱਕ ਜੀਨ-ਲੋਡਡ ਨੈਨੋਪਾਰਟੀਕਲ ਇੰਜੈਕਸ਼ਨ ਹੈ।ਇਹ ਖਾਸ ਤੌਰ 'ਤੇ ਠੋਸ ਟਿਊਮਰਾਂ ਨੂੰ ਮਾਰਨ ਲਈ ਰੇਟਰੋਵਾਇਰਲ ਵੈਕਟਰ ਦੁਆਰਾ ਨਿਸ਼ਾਨਾ ਸੈੱਲਾਂ ਵਿੱਚ ਸਾਈਕਲੀਨ G1 ਪਰਿਵਰਤਨਸ਼ੀਲ ਜੀਨ ਪੇਸ਼ ਕਰਦਾ ਹੈ।ਪ੍ਰਸ਼ਾਸਨ ਦਾ ਤਰੀਕਾ ਨਾੜੀ ਨਿਵੇਸ਼ ਹੈ.ਇੱਕ ਟਿਊਮਰ-ਨਿਸ਼ਾਨਾ ਦਵਾਈ ਦੇ ਰੂਪ ਵਿੱਚ ਜੋ ਸਰਗਰਮੀ ਨਾਲ ਮੈਟਾਸਟੈਟਿਕ ਕੈਂਸਰ ਸੈੱਲਾਂ ਦੀ ਖੋਜ ਅਤੇ ਨਸ਼ਟ ਕਰਦੀ ਹੈ, ਇਸਦਾ ਉਹਨਾਂ ਮਰੀਜ਼ਾਂ 'ਤੇ ਇੱਕ ਖਾਸ ਪ੍ਰਭਾਵ ਹੁੰਦਾ ਹੈ ਜੋ ਟਾਰਗੇਟਡ ਬਾਇਓਲੋਜਿਕਸ ਸਮੇਤ ਹੋਰ ਕੈਂਸਰ ਦਵਾਈਆਂ ਦੇ ਵਿਰੁੱਧ ਬੇਅਸਰ ਹਨ।
(2) ਨਿਓਵੈਸਕੁਲਜਨ
ਕੰਪਨੀ: ਮਨੁੱਖੀ ਸਟੈਮ ਸੈੱਲ ਸੰਸਥਾ ਦੁਆਰਾ ਵਿਕਸਤ ਕੀਤੀ ਗਈ।
ਸੂਚੀਕਰਨ ਦਾ ਸਮਾਂ: 7 ਦਸੰਬਰ, 2011 ਨੂੰ ਰੂਸ ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ, ਅਤੇ ਫਿਰ 2013 ਵਿੱਚ ਯੂਕਰੇਨ ਵਿੱਚ ਸੂਚੀਬੱਧ।
ਸੰਕੇਤ: ਪੈਰੀਫਿਰਲ ਧਮਣੀ ਰੋਗ ਦੇ ਇਲਾਜ ਲਈ, ਗੰਭੀਰ ਅੰਗ ischemia ਸਮੇਤ.
ਟਿੱਪਣੀਆਂ: ਨਿਓਵਾਸਕੁਲਜਨ ਇੱਕ ਡੀਐਨਏ ਪਲਾਜ਼ਮੀਡ-ਅਧਾਰਤ ਜੀਨ ਥੈਰੇਪੀ ਹੈ ਜਿਸ ਵਿੱਚ ਵੈਸਕੁਲਰ ਐਂਡੋਥੈਲਿਅਲ ਗਰੋਥ ਫੈਕਟਰ (ਵੀਈਜੀਐਫ) 165 ਜੀਨ ਨੂੰ ਪਲਾਜ਼ਮਿਡ ਰੀੜ੍ਹ ਦੀ ਹੱਡੀ ਉੱਤੇ ਬਣਾਇਆ ਜਾਂਦਾ ਹੈ ਅਤੇ ਮਰੀਜ਼ਾਂ ਵਿੱਚ ਦਾਖਲ ਕੀਤਾ ਜਾਂਦਾ ਹੈ।
(3) ਕੋਲੇਟਜੀਨ
ਕੰਪਨੀ: ਓਸਾਕਾ ਯੂਨੀਵਰਸਿਟੀ ਅਤੇ ਉੱਦਮ ਪੂੰਜੀ ਫਰਮਾਂ ਦੁਆਰਾ ਸਹਿ-ਵਿਕਸਤ।
ਸੂਚੀਕਰਨ ਦਾ ਸਮਾਂ: ਅਗਸਤ 2019 ਵਿੱਚ ਸੂਚੀਕਰਨ ਲਈ ਜਾਪਾਨੀ ਸਿਹਤ, ਕਿਰਤ ਅਤੇ ਭਲਾਈ ਮੰਤਰਾਲੇ ਦੁਆਰਾ ਮਨਜ਼ੂਰੀ ਦਿੱਤੀ ਗਈ।
ਸੰਕੇਤ: ਗੰਭੀਰ ਹੇਠਲੇ ਸਿਰੇ ਦੇ ischemia ਦਾ ਇਲਾਜ.
ਟਿੱਪਣੀਆਂ: ਕੋਲਾਟੇਜੀਨ ਇੱਕ ਪਲਾਜ਼ਮੀਡ-ਅਧਾਰਿਤ ਜੀਨ ਥੈਰੇਪੀ ਹੈ, ਐਂਜੇਸ ਦੁਆਰਾ ਤਿਆਰ ਕੀਤੀ ਪਹਿਲੀ ਮੂਲ ਜਪਾਨੀ ਜੀਨ ਥੈਰੇਪੀ ਦਵਾਈ।ਇਸ ਡਰੱਗ ਦਾ ਮੁੱਖ ਹਿੱਸਾ ਇੱਕ ਨੰਗਾ ਪਲਾਜ਼ਮੀਡ ਹੈ ਜਿਸ ਵਿੱਚ ਮਨੁੱਖੀ ਹੈਪੇਟੋਸਾਈਟ ਵਿਕਾਸ ਕਾਰਕ (HGF) ਦਾ ਜੀਨ ਕ੍ਰਮ ਹੁੰਦਾ ਹੈ।ਜੇ ਡਰੱਗ ਨੂੰ ਹੇਠਲੇ ਅੰਗਾਂ ਦੀਆਂ ਮਾਸਪੇਸ਼ੀਆਂ ਵਿੱਚ ਟੀਕਾ ਲਗਾਇਆ ਜਾਂਦਾ ਹੈ, ਤਾਂ ਪ੍ਰਗਟ ਕੀਤਾ HGF ਬੰਦ ਖੂਨ ਦੀਆਂ ਨਾੜੀਆਂ ਦੇ ਆਲੇ ਦੁਆਲੇ ਨਵੀਆਂ ਖੂਨ ਦੀਆਂ ਨਾੜੀਆਂ ਦੇ ਗਠਨ ਨੂੰ ਉਤਸ਼ਾਹਿਤ ਕਰੇਗਾ।ਕਲੀਨਿਕਲ ਅਜ਼ਮਾਇਸ਼ਾਂ ਨੇ ਅਲਸਰ ਨੂੰ ਸੁਧਾਰਨ ਵਿੱਚ ਇਸਦੀ ਪ੍ਰਭਾਵ ਦੀ ਪੁਸ਼ਟੀ ਕੀਤੀ ਹੈ।
END
ਪੋਸਟ ਟਾਈਮ: ਨਵੰਬਰ-10-2022